题目内容
某烃A的相对分子质量为78,不能使溴水褪色,0.5mol A完全燃烧时,得到27g水和67.2L二氧化碳(标准状况).
求:(1)A的结构简式.
(2)写出在催化剂作用下A与H2反应生成C.
求:(1)A的结构简式.
(2)写出在催化剂作用下A与H2反应生成C.
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:0.5mol A完全燃烧时,得到27g水和67.2L二氧化碳(标准状况),水的物质的量为1.5mol,二氧化碳的物质的量为3mol,根据原子守恒可知A的分子式为C6H6,烃A不能使溴水褪色,则A为苯,苯与氢气在催化剂、加热条件下与氢气发生加成反应生成环己烷.
解答:
解:(1)0.5mol A完全燃烧时,得到27g水和67.2L二氧化碳(标准状况),水的物质的量为
=1.5mol,二氧化碳的物质的量=
=3mol,根据原子守恒可知A的分子中C原子数目=
=6、H原子数目=
=6,故A的分子式为C6H6,烃A不能使溴水褪色,则A为苯,结构简式为: ,
,
答:烃A的结构简式为: ;
;
(2)苯与氢气在催化剂、加热条件下与氢气发生加成反应生成环己烷,反应方程式为: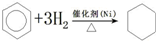 ,
,
答:催化剂作用下A与H2反应生成C的方程式为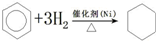 .
.
| 27g |
| 18g/mol |
| 67.2L |
| 222.4L/mol |
| 3mol |
| 0.5mol |
| 1.5mol×2 |
| 0.5mol |
 ,
,答:烃A的结构简式为:
 ;
;(2)苯与氢气在催化剂、加热条件下与氢气发生加成反应生成环己烷,反应方程式为:
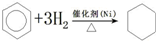 ,
,答:催化剂作用下A与H2反应生成C的方程式为
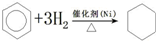 .
.
点评:本题考查有机物分子式与结构的确定,难度不大,注意理解掌握燃烧法利用原子守恒确定有机物的组成.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目
加热条件下,将24g CuO、Fe2O3的混合物与充足的CO完全反应,并将反应后的气体全部通入到澄清石灰水中,得到白色沉淀40g.下列有关叙述中正确的是( )
| A、原混合物中CuO与Fe2O3物质的量的比为l:l |
| B、反应后所得CO2的质量为8.8g |
| C、参加反应的CO的质量为8.4g |
| D、原混合物中CuO与Fe2O3的质量比为1:1 |
下列离子方程式正确的是( )
| A、NaHSO4与过量的Ba(OH)2溶液反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| B、碳酸氢铵溶液中加入过量氢氧化钠溶液 HCO3-+OH-=CO32-+H2O |
| C、碳酸镁溶于硝酸中:CO32-+2H+=H2O+CO2↑ |
| D、硫化钠溶于水中:S2-+2H2O=H2S↑+2OH- |
 如图,在密闭容器中反应:C(s)+H2O(g)?CO(g)+H2(g) (吸热反应)达到平衡后,由于条件的改变而引起正、逆反应速率的变化,及平衡移动状况,则改变的条件是( )
如图,在密闭容器中反应:C(s)+H2O(g)?CO(g)+H2(g) (吸热反应)达到平衡后,由于条件的改变而引起正、逆反应速率的变化,及平衡移动状况,则改变的条件是( )| A、增加CO浓度 | B、增大压强 |
| C、升高温度 | D、增加水蒸气 |