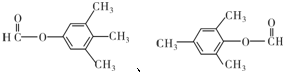题目内容
8. 瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池示意图如右,该燃料电池工作时,外电路中电子的流动方向是从电极1到电极2;电池的总反应为4NH3+3O2=2N2+6H2O.
瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池示意图如右,该燃料电池工作时,外电路中电子的流动方向是从电极1到电极2;电池的总反应为4NH3+3O2=2N2+6H2O.
分析 在燃料电池的负极上发生燃料氨气失电子的氧化反应,则电子从电极1经外电路到电极2,氧气在电极2得电子发生还原反应,电池的总反应为4NH3+3O2=2N2+6H2O.
解答 解:在燃料电池的负极上发生燃料氨气失电子的氧化反应,则碱性环境下电极1发生的电极反应为:2NH3+6OH--6e-=N2↑+6H2O,电子从电极1经外电路到电极2,氧气在电极2得电子发生还原反应,碱性条件下,氧气在正极生成氢氧根离子,其电极反应为:O2+2H2O+4e-=4OH-,电池的总反应为4NH3+3O2=2N2+6H2O,故答案为:1;2;4NH3+3O2=2N2+6H2O.
点评 本题考查了原电池原理,注意燃料电池的工作原理和规律:负极上是燃料失电子的氧化反应,在正极上氧气发生得电子的还原反应,题目难度不大.

练习册系列答案
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案
相关题目
16.化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
| A. | 二氧化碳的结构式:O-C-O | B. | 羟基的电子式为: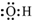 | ||
| C. | 丙烷分子的球棍模型: | D. | 硫离子的结构示意图: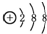 |
3.下列陈述Ⅰ、Ⅱ均正确且具有因果关系的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | SO2有漂白性 | SO2可使溴水褪色 |
| B | NH3具有碱性 | NH3极易溶于水 |
| C | 浓硫酸有吸水性 | 用浓硫酸干燥SO2 |
| D | HNO3具有酸性 | 可用铁和稀HNO3制取氢气 |
| A. | A | B. | B | C. | C | D. | D |
13.下列关于化学用语的表述正确的是( )
| A. | 原子核内有8个中子的碳原子${\;}_{8}^{14}$C | |
| B. | 基态氧原子核外电子的轨道表示式: | |
| C. | HClO的结构式为H-Cl-O | |
| D. | Ca2+的结构示意图为 ,NH4Cl的电子式为 ,NH4Cl的电子式为 |
17.在稀硫酸中加入铜粉,铜粉不溶,再加入下列固体粉末:①FeCl2; ②Fe2O3③Zn;④KNO3; ⑤HCl; 铜粉可溶解的是( )
| A. | ①②⑤ | B. | ②④ | C. | ②③⑤ | D. | 只有④ |

 探究上述四种酸的氧化性相对强弱及其与铜反应的还原产物的性质:
探究上述四种酸的氧化性相对强弱及其与铜反应的还原产物的性质:
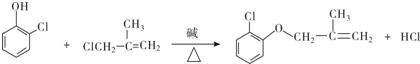 (有机物用结构简式表示,下同).
(有机物用结构简式表示,下同).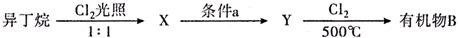
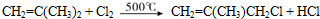 ;
;