题目内容
把2.16g某有机物在纯氧中完全燃烧,依次通入装有无水氯化钙干燥管和澄清石灰水,无水氯化钙干燥管增重1.44g,通过澄清石灰水得到沉淀14g.又知此有机物蒸气0.224L(已折算成标准状况下)的质量为1.08g.
(1)求此有机物的分子量?
(2)求此有机物的分子式?
(3)若此有机物跟FeCl3溶液作用显紫色,写出此有机物可能的结构简式.
(1)求此有机物的分子量?
(2)求此有机物的分子式?
(3)若此有机物跟FeCl3溶液作用显紫色,写出此有机物可能的结构简式.
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:(1)根据分子式可确定分子量;
(2)有机物燃烧的产物二氧化碳质量可以根据和澄清石灰水反应得到沉淀的质量来获得,无水氯化钙干燥管增加的质量是水的质量,根据原子守恒来确定有机物的组成情况即可;
(2)有机物跟FeCl3溶液作用显紫色,说明含有酚羟基,根据同分异构体的概念来书写.
(2)有机物燃烧的产物二氧化碳质量可以根据和澄清石灰水反应得到沉淀的质量来获得,无水氯化钙干燥管增加的质量是水的质量,根据原子守恒来确定有机物的组成情况即可;
(2)有机物跟FeCl3溶液作用显紫色,说明含有酚羟基,根据同分异构体的概念来书写.
解答:
解:有机物蒸气0.224L即0.01mol(已折算成标准状况下)的质量为1.08g,所以有机物的M=
=108g/mol,无水氯化钙干燥管增重1.44g,即有机物燃烧生成的水的质量是1.44g,所以水的物质的量是
=0.08mol,通过澄清石灰水得到沉淀14g,即0.14mol,所以生成二氧化碳的物质的量是0.14mol,根据原子守恒,2.16g即0.02mol有机物中含有碳原子为0.14mol,含有氢原子是0.16mol,所以碳原子数是7,氢原子数是8,根据相对分子质量,得出含有的氧原子个数是1,即分子式为:C7H8O,
(1)此有机物的分子式为C7H8O,分子量为108;
答;此有机物的分子量为108;
(2)根据以上分析此有机物的分子式为C7H8O;
答:此有机物的分子式为C7H8O;
(3)此有机物跟FeCl3溶液作用显紫色,说明含有酚羟基,得出符合条件的同分异构体的结构简式有: ,
,
答:此有机物可能的结构简式为 .
.
| 1.08g |
| 0.01mol |
| 1.44g |
| 18g/mol |
(1)此有机物的分子式为C7H8O,分子量为108;
答;此有机物的分子量为108;
(2)根据以上分析此有机物的分子式为C7H8O;
答:此有机物的分子式为C7H8O;
(3)此有机物跟FeCl3溶液作用显紫色,说明含有酚羟基,得出符合条件的同分异构体的结构简式有:
 ,
,答:此有机物可能的结构简式为
 .
.
点评:本题考查学生有机物的分子式的确定知识,注意原子守恒思想的灵活应用是关键,难度不大.

练习册系列答案
 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
浙江海洋经济发展示范区建设已上升为国家战略,海洋经济将成为浙江经济转型升级发展的重点.下列说法不正确的是( )
| A、从海水中提取氯化钠的过程涉及化学反应 |
| B、从海带中提取碘单质的过程涉及置换反应 |
| C、从海水中提取溴单质的过程涉及氧化还原反应 |
| D、海水中含有氯化钠等多种氯化物;除了氯,海水中溴的储量也很高,溴也被称为“海洋元素” |
如图所示,y表示沉淀的量,x表示加试剂的体积,能够用该图表示的反应是( )


| A、向Ca(OH)2溶液中通人CO2至过量 |
| B、在盐酸和硫酸的混合溶液中加入Ba(OH)2溶液至过量 |
| C、在水玻璃和烧碱混合溶液中加入盐酸至过量 |
| D、在Ba(OH)2溶液中加入氯化铝溶液至过量 |
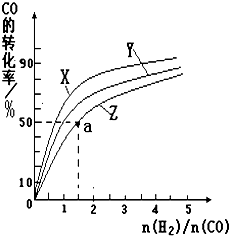 甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产.工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:
甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产.工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为: (1)在短周期主族元素中,氯及其相邻元素的电负性由大到小的顺序是
(1)在短周期主族元素中,氯及其相邻元素的电负性由大到小的顺序是