题目内容
11.A、B、C、D、E、F、G七种短周期元素的原子序数依次增大.其中仅有一种稀有气体元素.A和E最外层电子数相同,短周期主族元素的原子中,E原子的半径最大;B、C和F 在周期表中相邻,B、C同周期,C、F同主族,F原子的质子数是C原子质子数的2倍;A和C可形成两种常见的液态化合物X和Y(相对分子质量X<Y );D形成的分子为单原子分子.回答问题:(1)Y的电子式为
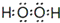 .
.(2)液态化合物Y与稀硫酸酸化的K2Cr2O7溶液作用可产生一种无色助燃气体及可溶性的Cr2(SO4)3,则该反应的离子方程式为Cr2O72-+3H2O2+8H+=2Cr3++3O2+7H2O.
(3)用某种金属易拉罐与A、C、E组成的化合物的水溶液反应.产生的气体可充填气球,请写出该反应的离子方程式2Al+2OH-+2H2O=2AlO2-+3H2↑,使用这种气球存在的隐患是氢气易燃、易爆.
(4)P和Q两种物质都是由A、C、E、F四种元素组成的盐,其水溶液都显酸性,等物质的量的P和Q恰好完全反应.写出该反应的离子方程式:H++HSO3-═SO2↑+H2O,这两种盐均含有的化学键类型为离子键、共价键.
(5)由A、B两元素形成的化合物W可作为火箭推进器中的强还原剂,已知一个W分子和一个Y分子中都含有18个电子,1mol液态W和2mol液态Y恰好完全反应.写出该反应的化学方程式为N2H4+2H2O2=N2+4H2O.
分析 A、B、C、D、E、F、G七种短周期主族元素的原子序数依次增大.A和E最外层电子数相同,二者同主族,短周期主族元素的原子中,E原子的半径最大,则E为Na;B、C和F在周期表中相邻,B、C同周期,C、F同主族,则B、C处于第二周期,F处于第三周期,F原子的质子数是C原子质子数的2倍,则C为O元素、F为S元素,可知B为N元素;A和C可形成两种常见的液态化合物X和Y(相对分子质量X<Y ),则A为H元素,X为H2O、Y为H2O2;D形成的分子为单原子分子,且原子序数介于氧、钠之间,故D为Ne元素;G的原子序数大于硫,故G为Cl,据此解答.
解答 解:A、B、C、D、E、F、G七种短周期主族元素的原子序数依次增大.A和E最外层电子数相同,二者同主族,短周期主族元素的原子中,E原子的半径最大,则E为Na;B、C和F在周期表中相邻,B、C同周期,C、F同主族,则B、C处于第二周期,F处于第三周期,F原子的质子数是C原子质子数的2倍,则C为O元素、F为S元素,可知B为N元素;A和C可形成两种常见的液态化合物X和Y(相对分子质量X<Y ),则A为H元素,X为H2O、Y为H2O2;D形成的分子为单原子分子,且原子序数介于氧、钠之间,故D为Ne元素;G的原子序数大于硫,故G为Cl.
(1)Y为H2O2,电子式为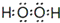 ,故答案为:
,故答案为: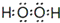 ;
;
(2)Y为H2O2,被K2Cr2O7氧化为氧气,反应的离子方程式是Cr2O72-+3H2O2+8H+=2Cr3++3O2+7H2O,
故答案为:Cr2O72-+3H2O2+8H+=2Cr3++3O2+7H2O;
(3)A、C、E组成的化合物的水溶液为NaOH溶液,金属易拉罐含铝,则发生的离子反应为2Al+2OH-+2H2O=2AlO2-+3H2↑,生成的氢气易燃、易爆,则存在安全隐患,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;氢气易燃、易爆;
(4)P和Q两种物质都是由H、O、Na、S四种元素组成的盐,其水溶液都显酸性,两物质为NaHSO3、NaHSO4,等物质的量的P和Q恰好完全反应,该反应的离子方程式:H++HSO3-═SO2↑+H2O,硫酸氢钠和亚硫酸氢钠中均含有离子键和共价键,
故答案为:H++HSO3-═SO2↑+H2O;离子键和共价键;
(5)由A、B两元素形成的化合物W,一个W分子和一个Y分子中都含有18个电子,1mol液态W和2mol液态Y恰好完全反应,该反应方程式为:N2H4+2H2O2=N2+4H2O,
故答案为:N2H4+2H2O2=N2+4H2O.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,注意对元素化合物性质的掌握,难度中等.

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案| A. | KCl | B. | HF | C. | NaOH | D. | CaCl2 |
(1)C、Si、N的电负性由大到小的顺序是N>C>Si.C60和金刚石都是碳的同素异形体,二者比较,熔点高的是金刚石.
(2)A、B均为短周期金属元素,依据如表数据,写出B的基态原子的电子排布式1S22S22P63S2.
| 电离能 /(kJ•mol-1) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
(4)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等.
①每个COCl2分子内含有3个σ键,1个π键.其中心原子采取SP2杂化轨道方式.
②配合物Fe(CO)5的配体是CO.
| A. | N2和NH3的质量分数相等 | |
| B. | N2、H2、NH3的浓度之比为1:3:2 | |
| C. | 当断开1mol氮氮三键的同时,断开3mol氢氢键 | |
| D. | 氮气的体积分数保持不变 |
| A. | 三种元素的最高正化合价中,Z的最大 | |
| B. | W晶体中只存在有共价键 | |
| C. | 原子半径:X>Y>Z | |
| D. | Y的最高价氧化物对应的水化物是强酸 |
| A. | ${\;}_{78}^{202}$ Pt和${\;}_{78}^{198}$Pt的中子数相同,互称为同位素 | |
| B. | ${\;}_{78}^{202}$ Pt和${\;}_{78}^{198}$Pt的质子数相同,互称为同位素 | |
| C. | ${\;}_{78}^{202}$ Pt和${\;}_{78}^{198}$Pt不能互称为同位素 | |
| D. | ${\;}_{78}^{202}$Pt和${\;}_{78}^{198}$Pt是同一种核素 |
| A. | NaHCO3 | B. | CH3COOH | C. | C6H12O6 | D. | Na2CO3 |
 ; ②Cl2
; ②Cl2 ;③CO2
;③CO2 .
.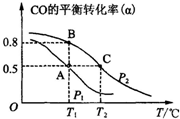 利用CO和H2合成甲醇,其反应的化学方程式为CO(g)+2H2(g)?CH3OH(g).今在一容积可变的密闭容器中,充有10mol CO和20mol H2用于合成甲醇.CO的平衡转化率(α)与温度(T)、压强(P)的关系如图所示:
利用CO和H2合成甲醇,其反应的化学方程式为CO(g)+2H2(g)?CH3OH(g).今在一容积可变的密闭容器中,充有10mol CO和20mol H2用于合成甲醇.CO的平衡转化率(α)与温度(T)、压强(P)的关系如图所示: