题目内容
6.对于达到平衡状态的可逆反应:N2+3H2?2NH3,下列有关叙述正确的是( )| A. | N2和NH3的质量分数相等 | |
| B. | N2、H2、NH3的浓度之比为1:3:2 | |
| C. | 当断开1mol氮氮三键的同时,断开3mol氢氢键 | |
| D. | 氮气的体积分数保持不变 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、当反应达到平衡状态时,N2和NH3的质量分数不变,而不是相等,故A错误;
B、当体系达平衡状态时,N2、H2、NH3的浓度之比为1:3:2,也可能不是,与各物质的初始浓度及转化率有关,故B错误;
C、当断开1mol氮氮三键的同时,断开3mol氢氢键,都反映的正反应方向,未体现正与逆的关系,故C错误;
D、氮气的体积分数保持不变,说明各物质的量不变,达平衡状态,故D正确;
故选D.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
相关题目
16.足量的锌和下列酸反应,产生H2的物质的量最多的是( )
| A. | 10mL 18.4mol/L H2SO4 | B. | 30mL 3mol/L盐酸 | ||
| C. | 30mL 2mol/L H2SO4 | D. | 30mL 5mol/L HNO3 |
17.下列实验不能获得预期目的是( )
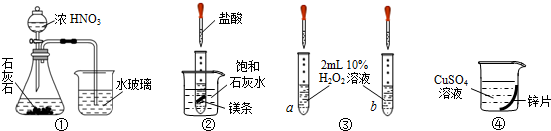

| A. | 实验①烧杯中出现白色胶状沉淀,证明非金属性:N>C>Si | |
| B. | 实验②烧杯中出现白色浑浊,说明镁与盐酸反应是放热反应 | |
| C. | 实验③a、b分别滴加2滴FeCl3溶液、CuSO4溶液,验证不同催化剂对反应速率的影响 | |
| D. | 实验④利用置换反应,证明金属单质还原性强弱,判断金属性强弱 |
14.下列说法错误的是( )
| A. | 酚类化合物有毒,不能用于杀菌消毒 | |
| B. | 乙烯可催熟水果 | |
| C. | 石油的裂解可获得乙烯、丙烯等短链烯烃 | |
| D. | 甲醛的水溶液可用于防腐 |
18.下列关于物质性质递变规律的叙述不正确的是( )
| A. | 原子的还原性:K>Na>Mg>Al | |
| B. | 氢化物的稳定性:HCl<H2S<PH3<SiH4 | |
| C. | 酸性:H2CO3<H3PO4<H2SO4<HClO4 | |
| D. | 原子的氧化性:F>Cl>S>P |
15.下列各组中,含有离子晶体、分子晶体、原子晶体各一种的是( )
| A. | KCl、HCl、S | B. | 金刚石、Na3PO4、MgO | ||
| C. | HF、SiC、Ar | D. | H2O、SiO2、K2CO3 |
16.下列化学式仅代表一种物质的是( )
| A. | CH4 | B. | C3H8 | C. | C4H10 | D. | C5H12 |
 ;
; 的系统名称为:3,4,4一三甲基一l一戊炔
的系统名称为:3,4,4一三甲基一l一戊炔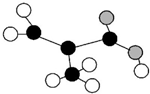 所示(图中球与球之间的连线代表化学键,如单键、双键等).该分子的结构简式为
所示(图中球与球之间的连线代表化学键,如单键、双键等).该分子的结构简式为 .
.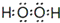 .
.