题目内容
3.W是由短周期元素X、Y、Z组成的盐.X、Y、Z原子的最外层电子数依次增大,Z原子最外层电子数是内层电子数的3倍;X、Y原子最外层电子数之和等于Z原子的最外层电子数;Y、Z同周期且相邻,但与X不同周期.下列说法一定正确的是( )| A. | 三种元素的最高正化合价中,Z的最大 | |
| B. | W晶体中只存在有共价键 | |
| C. | 原子半径:X>Y>Z | |
| D. | Y的最高价氧化物对应的水化物是强酸 |
分析 W是由短周期元素X、Y、Z组成的盐,X、Y、Z原子的最外层电子数依次增大,Z原子最外层电子数是内层电子数的3倍,最外层电子数不超过8个,所以其内层为K层,则Z为O元素;X、Y原子最外层电子数之和等于Z原子的最外层电子数,则X和Y最外层电子数之和为6;Y、Z同周期且相邻,Y原子序数小于Z,所以Y是N元素,但Y与X不同周期,则X是H元素或Na元素,则W为NH4NO3或NH4NO2、NaNO3或NaNO2,
A.主族元素最高正化合价等于其族序数,但O、F元素除外;
B.硝酸铵为强酸弱碱盐;
C.原子电子层数越多其原子半径越大,同一周期元素,其原子半径随着原子序数增大而减小;
D.Y是N元素,其最高价氧化物的水化物是硝酸.
解答 解:W是由短周期元素X、Y、Z组成的盐,X、Y、Z原子的最外层电子数依次增大,Z原子最外层电子数是内层电子数的3倍,最外层电子数不超过8个,所以其内层为K层,则Z为O元素;X、Y原子最外层电子数之和等于Z原子的最外层电子数,则X和Y最外层电子数之和为6;Y、Z同周期且相邻,Y原子序数小于Z,所以Y是N元素,但Y与X不同周期,则X是H元素或Na元素,则W为NH4NO3或NH4NO2、NaNO3或NaNO2,
A.主族元素最高正化合价等于其族序数,但O、F元素除外,所以这三种元素最高正化合价中Y的最大,故A错误;
B.W是硝酸铵,为铵盐,结构中既存在共价键又有离子键,故B错误;
C.原子电子层数越多其原子半径越大,同一周期元素,其原子半径随着原子序数增大而减小,如果X是H元素,则原子半径Y>Z>X,如果X是Na元素,则原子半径X>Y>Z,故C错误;
D.Y是N元素,其最高价氧化物的水化物是硝酸,硝酸是强酸,故D正确;
故选D.
点评 本题考查原子结构和元素周期律,为高频考点,侧重考查学生分析判断能力,涉及盐的性质、元素的化合价、元素周期律等知识点,明确元素周期律及元素化合物性质是解本题关键,注意规律中的反常现象,易错选项是A.

①乙烯 ②苯 ③乙醇 ④甲烷 ⑤乙酸 ⑥二氧化硫.
| A. | ①②③④⑤ | B. | ①③⑥ | C. | ②④⑤ | D. | ②④⑤⑥ |
| A. | 酚类化合物有毒,不能用于杀菌消毒 | |
| B. | 乙烯可催熟水果 | |
| C. | 石油的裂解可获得乙烯、丙烯等短链烯烃 | |
| D. | 甲醛的水溶液可用于防腐 |
| A. | 原子的还原性:K>Na>Mg>Al | |
| B. | 氢化物的稳定性:HCl<H2S<PH3<SiH4 | |
| C. | 酸性:H2CO3<H3PO4<H2SO4<HClO4 | |
| D. | 原子的氧化性:F>Cl>S>P |
| A. | CaCl2 | B. | H2O2 | C. | Na2S | D. | NaOH |
| A. | KCl、HCl、S | B. | 金刚石、Na3PO4、MgO | ||
| C. | HF、SiC、Ar | D. | H2O、SiO2、K2CO3 |
| A. | 2甲基丙烷 | B. | 2甲基丁烷 | C. | 2,2二甲基丙烷 | D. | 2,3二甲基丁烷 |
| A. | “玉兔”月球车上的太阳能电池的材料是硅酸盐 | |
| B. | 利用二氧化碳制造全降解塑料,可以消除温室效应 | |
| C. | 实验室镁着火时,可使用泡沫灭火器灭火 | |
| D. | 可使用氢氧化钠溶液鉴别大豆油与矿物油 |
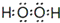 .
.