题目内容
2.含有共价键的离子化合物是( )| A. | KCl | B. | HF | C. | NaOH | D. | CaCl2 |
分析 活泼金属和活泼非金属元素直接易形成离子键,非金属元素之间易形成共价键,含有离子键的化合物是离子化合物,离子化合物中可能含有共价键.
解答 解:A.KCl中钾离子和氯离子之间只存在离子键,为离子化合物,故A错误;
B.HF分子中H-F原子之间存在共价键,为共价化合物,故B错误;
C.NaOH中钠离子和氢氧根离子之间存在离子键、O-H原子之间存在共价键,故C正确;
D.氯化钙中钙离子和氯离子之间只存在离子键,为离子化合物,故D错误;
故选C.
点评 本题考查离子化合物和共价化合物的判断,为高频考点,明确离子键和共价键根本区别是解本题关键,注意D中不含共价键,为易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.下列物质中能使酸性KMnO4溶液褪色的是( )
①乙烯 ②苯 ③乙醇 ④甲烷 ⑤乙酸 ⑥二氧化硫.
①乙烯 ②苯 ③乙醇 ④甲烷 ⑤乙酸 ⑥二氧化硫.
| A. | ①②③④⑤ | B. | ①③⑥ | C. | ②④⑤ | D. | ②④⑤⑥ |
17.下列实验不能获得预期目的是( )
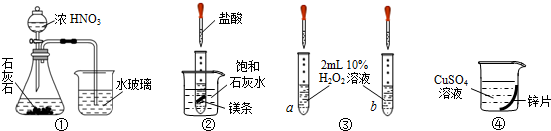

| A. | 实验①烧杯中出现白色胶状沉淀,证明非金属性:N>C>Si | |
| B. | 实验②烧杯中出现白色浑浊,说明镁与盐酸反应是放热反应 | |
| C. | 实验③a、b分别滴加2滴FeCl3溶液、CuSO4溶液,验证不同催化剂对反应速率的影响 | |
| D. | 实验④利用置换反应,证明金属单质还原性强弱,判断金属性强弱 |
7.下列反应的离子方程式表示正确的是( )
| A. | H2O2溶液与酸性KMnO4溶液反应:2MnO4-+3H2O2+6H+═2Mn2++6H2O+4O2↑ | |
| B. | 向Fe(NO3)3溶液中加入过量的HI溶液:2 NO3-+8H++6I-═3I2+2NO↑+4H2O | |
| C. | 少量SO2通入碳酸钠溶液中:CO32-+SO2═CO2+S O32- | |
| D. | 0.01 mol•L-1 NH4Al(SO4)2溶液与0.02 mol•L-1 Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+Al(OH)3↓+NH3•H2O |
14.下列说法错误的是( )
| A. | 酚类化合物有毒,不能用于杀菌消毒 | |
| B. | 乙烯可催熟水果 | |
| C. | 石油的裂解可获得乙烯、丙烯等短链烯烃 | |
| D. | 甲醛的水溶液可用于防腐 |
12.下列烷烃中,既能由烯烃加氢得到也能由炔烃加氢得到的是( )
| A. | 2甲基丙烷 | B. | 2甲基丁烷 | C. | 2,2二甲基丙烷 | D. | 2,3二甲基丁烷 |
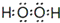 .
.