题目内容
1.写出下列物质的电子式:①MgCl2
 ; ②Cl2
; ②Cl2 ;③CO2
;③CO2 .
.
分析 ①氯化镁为离子化合物,必须标出阴阳离子的电子式;
②氯气中存在1对氯氯共用电子对,氯原子最外层达到8电子稳定结构;
③二氧化碳中存在两个碳氧双键,C、O原子最外层都达到最外层8个电子.
解答 解:①氯化镁为离子化合物,化学式中存在阴阳离子,其电子式中需要标出阴阳离子所带电荷,氯化镁的电子式为: ,
,
故答案为: ;
;
②Cl2的电子式为: ,故答案为:
,故答案为: ;
;
③二氧化碳中存在两对碳氧共用电子对,二氧化碳的电子式为: ,故答案为:
,故答案为: .
.
点评 本题考查了电子式的书写,题目难度不大,注意掌握电子式的概念及书写原则,明确离子化合物与共价化合物的电子式表示方法及区别.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
9.可逆反应:3A(g)+B(g)?2C(g)+2D(g) 在不同条件下的反应速率分别为:
(1)v(A)=0.6mol•L-1•min-1 (2)v(B)=0.007mol•L-1•S-1
(3)v(C)=0.4mol•L-1•min-1 (4)v(D)=0.80mol•L-1•min-1
此反应在不同条件下进行最快的是( )
(1)v(A)=0.6mol•L-1•min-1 (2)v(B)=0.007mol•L-1•S-1
(3)v(C)=0.4mol•L-1•min-1 (4)v(D)=0.80mol•L-1•min-1
此反应在不同条件下进行最快的是( )
| A. | (1) | B. | (2) | C. | (3) | D. | (4) |
16.足量的锌和下列酸反应,产生H2的物质的量最多的是( )
| A. | 10mL 18.4mol/L H2SO4 | B. | 30mL 3mol/L盐酸 | ||
| C. | 30mL 2mol/L H2SO4 | D. | 30mL 5mol/L HNO3 |
13.下列物质中能使酸性KMnO4溶液褪色的是( )
①乙烯 ②苯 ③乙醇 ④甲烷 ⑤乙酸 ⑥二氧化硫.
①乙烯 ②苯 ③乙醇 ④甲烷 ⑤乙酸 ⑥二氧化硫.
| A. | ①②③④⑤ | B. | ①③⑥ | C. | ②④⑤ | D. | ②④⑤⑥ |
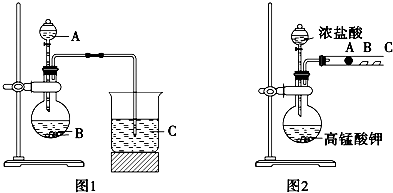
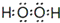 .
.