题目内容
10.海洋中有丰富的“食品、矿产、能源、药物和水产资源”等,下列说法正确的是( )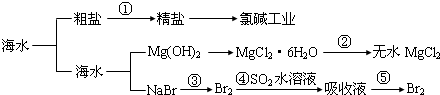
| A. | 第①步中除去泥沙及Ca2+、Mg2+等杂质时,不涉及化学变化过程 | |
| B. | 工业上,通过电解“精盐”水溶液可以制取金属钠 | |
| C. | 第②步的反应条件是“在空气中直接加热” | |
| D. | 第③、④、⑤步中均涉及氧化还原反应 |
分析 海水通过蒸发浓缩得到粗盐和母液,粗盐精制除去杂质得到精盐,电解饱和食盐水得到氢氧化钠、氯气和氢气,母液中含有镁离子和溴离子,加入石灰乳沉淀镁离子过滤得到氢氧化镁沉淀和滤液,氢氧化镁溶解后浓缩蒸发,冷却结晶,过滤洗涤,在氯化氢气流中加热失去结晶水得到无水氯化镁,滤液中加入氧化剂氯水氧化溴离子为溴单质,再通入二氧化硫吸收后,加入酸重新生成溴单质,
A.第①步中除去泥沙是物理变化,除去Ca2+、Mg2+等杂质时需要加入碱、盐沉淀离子发生化学反应;
B.电解氯化钠溶液得到氢氧化钠、氯气和水,不能得到金属钠;
C.氯化镁晶体加热时氯化镁会溶解在水中水解生成氢氧化镁,不能得到氯化镁固体;
D.第③步将溴离子被氧化为溴单质,第④步中溴单质被还原为溴离子,第⑤步中溴离子被氧化为溴单质;
解答 解:A.第①步中除去泥沙是物理变化,除去Ca2+、Mg2+等杂质时需要加入碳酸钠、碱氢氧化钠发生化学反应生成碳酸钙沉淀、氢氧化镁沉淀过滤除去,是化学变化,故A错误;
B.钠是活泼金属,工业上,通过电解熔融氯化钠可以制取金属钠,故B错误;
C.氯化镁晶体加热时氯化镁会溶解在水中水解生成氢氧化镁,应在氯化氢气流中防止氯化镁水解,加热失去结晶水,故C错误;
D.第③步将溴离子被氧化为溴单质,第④步中溴单质被还原为溴离子,第⑤步中溴离子被氧化为溴单质,故D正确;
故选D.
点评 本题考查了海水的利用,物质的提纯和分离方法,利用所学知识结合框图信息是解答本题的关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.在一密闭容器中充入1molH2和1molI2,压强为p(Pa),并在一定温度下使其发生反应,H2(g)+I2(g)?2HI(g)△H<0,下列说法正确的是( )
| A. | 保持容器容积不变,向其加入1molH2(g),反应速率一定加快 | |
| B. | 保持容器容积不变,向其中加入1molN2(N2不参加反应),反应速率一定加快 | |
| C. | 保持容器内气体压强不变,向其中加入1molN2(N2不参加反应),反应速率一定加快 | |
| D. | 保持容器内气体压强不变,向其中加入1molH2(g)和1molI2(g),反应速率一定加快 |
18.下列化学反应的离子方程式正确的是( )
| A. | 氢氧化镁中滴加盐酸:H++OH-═H2O | |
| B. | Cl2通入水中:Cl2+H2O═2 H++Cl-+ClO- | |
| C. | 金属铝溶于氢氧化钠溶液:2Al+6OH-═2AlO2-+3H2↑ | |
| D. | 用FeCl3溶液腐蚀铜电路板:2Fe3++Cu═2Fe2++Cu2+ |
5.在某无色透明的酸性溶液中,能大量共存的离子组是( )
| A. | Na+、K+、SO42-、HCO3- | B. | Na+、K+、Cl?、SO42- | ||
| C. | Cu2+、K+、SO42-、NO3- | D. | Fe2+、K+、NO3-、Cl? |
15.氢化钠与水反应:NaH+H2O=NaOH+H2↑,对该反应的描述正确的是( )
| A. | NaH是氧化剂 | B. | H2O是氧化剂 | ||
| C. | 氧化剂与还原剂的质量比为1:1 | D. | 每生成1molH2转移2mol电子 |
2.下列有关实验装置进行的相应实验,能达到实验目的是( )
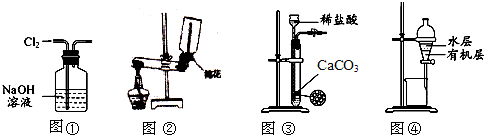

| A. | 用图①所示装置除去Cl2中含有的少量HCl | |
| B. | 用图②所示装置制备并收集O2 | |
| C. | 用图③所示装置制取少量的CO2气体 | |
| D. | 用图④所示装置分离汽油萃取碘水后已分层的有机层和水层 |


 .
. .
.