题目内容
19.有机物A的蒸汽密度为6.7g•L-1(已折算为标况),现取15g A完全氧化,产物依次通过浓硫酸和碱石灰,浓硫酸增重9g,碱石灰增重39.6g.用现代物理方法测定:①核磁共振仪测出A的核磁共振氢谱有5组峰,其峰面积之比为1:2:2:2:3.
②利用红外光谱仪可初步检测有机化合物中的某些基团,现测得A分子中具有一个苯环结构,一个C-O-C结构和一个C=O结构,且A的苯环上只有一取代基.
③性质实验证明,A能在稀硫酸作用下生成两种有机物,且其中一种有酸性.
(1)通过计算求A的相对分子质量及分子式.
(2)根据谱图信息写出A的三种可能结构.
分析 (1)根据M=ρVm计算有机物的摩尔质量,可以确定相对分子质量,浓硫酸增重9g为水的质量,碱石灰增重39.6g为生成二氧化碳,计算二氧化碳和水的物质的量,根据原子守恒计算A分子中C、H原子数目,再结合相对分子质量确定氧原子数目,进而确定分子式;
(2)A能在稀硫酸作用下生成两种有机物,且其中一种有酸性,说明A含有酯基,再结合红外光谱特征、核磁共振氢谱确定可能的结构简式.
解答 解:(1)有机物A的蒸汽密度为6.7g•L-1(已折算为标况),则其摩尔质量为22.4L/mol×6.7g/L=150g/mol,故A的相对分子质量为150;
15g A的物质的量为$\frac{15g}{150g/mol}$=0.1mol,把燃烧产物通过浓硫酸和碱石灰,浓硫酸增重9g,则生成水的物质的量是$\frac{9g}{18g/mol}$=0.5mol,碱石灰增重39.6g,则生成二氧化碳的物质的量是$\frac{39.6g}{44g/mol}$=0.9mol,故分子中N(C)=$\frac{0.9mol}{0.1mol}$=9、N(H)=$\frac{0.5mol×2}{0.1mol}$=10,则N(O)=$\frac{150-12×9-10}{16}$=2,A的分子式为C9H10O2,
答:A的相对分子质量为150,分子式为C9H10O2.
(2)A能在稀硫酸作用下生成两种有机物,且其中一种有酸性,说明A含有酯基,A的核磁共振氢谱有5组峰,既含有5种类型的氢原子,其峰面积之比为1:2:2:2:3,既5种氢原子的个数之比是1:2:2:2:3,A分子中具有一个苯环结构,一个C-O-C结构和一个C=O结构,且A的苯环上只有一取代基,则A的结构简式为: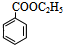 、
、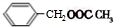 、
、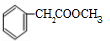 ,
,
答:A可能的结构简式为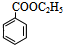 、
、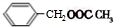 、
、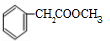 .
.
点评 本题考查有机物分子式与结构的确定、同分异构体书写等,难度中等,掌握燃烧法利用原子守恒确定有机物的分子式,熟练掌握官能团的性质与转化.

 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案| A. | HCl | B. | H2CO3 | C. | H2SO4 | D. | CH3COOH |
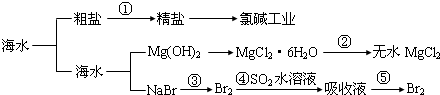
| A. | 第①步中除去泥沙及Ca2+、Mg2+等杂质时,不涉及化学变化过程 | |
| B. | 工业上,通过电解“精盐”水溶液可以制取金属钠 | |
| C. | 第②步的反应条件是“在空气中直接加热” | |
| D. | 第③、④、⑤步中均涉及氧化还原反应 |
| A. | AlCl3溶液 | B. | NaHCO3溶液 | C. | NH4HCO3溶液 | D. | Fe2(SO4)3溶液 |
| A. | 锌和稀硫酸反应时,加入少量的CuSO4溶液可使反应加快 | |
| B. | 红热的铁丝与冷水接触,表面表成蓝黑色保护层 | |
| C. | 镀锌铁表面锌有划损时,仍然能阻止铁被氧化 | |
| D. | 在空气中金属铝表面迅速氧化形成保护层 |
| A. | 电离常数Ka | B. | 化学平衡常数K | ||
| C. | 水的离子积常数Kw | D. | 盐的水解常数Kh |
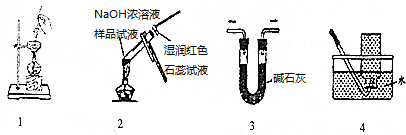
| A. | 用1从碘水中分离出碘 | B. | 用2检验试液中NH4+的存在 | ||
| C. | 用3干燥SO2气体 | D. | 用4收集HCl气体 |
| A. | 3:2 | B. | 1:2 | C. | 2:1 | D. | 2:3 |
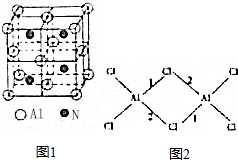
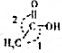 ,CH3COOH分子中σ键与π键个数之比7:1,分子中键角1<键角2(填“>”、“=”或“<”).
,CH3COOH分子中σ键与π键个数之比7:1,分子中键角1<键角2(填“>”、“=”或“<”).