题目内容
6.某有机物的蒸气完全燃烧时需三倍于其体积的氧气,产生二倍于其体积的CO2,该有机物可能是( )| A. | C2H4O | B. | C2H5OH | C. | CH3CHO | D. | CH3COOH |
分析 有机物蒸气完全燃烧,产生二倍于其体积的二氧化碳,则分子中含有2个C原子,对于烃含氧衍生物CxHyOz,1mol耗氧量为(x+$\frac{y}{4}$-$\frac{z}{2}$)mol,有机物蒸气完全燃烧时需三倍于其体积的氧气,则(x+$\frac{y}{4}$-$\frac{z}{2}$)=3,结合各选项中分子式进行判断.
解答 解:有机物蒸气完全燃烧,产生二倍于其体积的二氧化碳,则分子中含有2个C原子,对于烃含氧衍生物CxHyOz,1mol耗氧量为(x+$\frac{y}{4}$-$\frac{z}{2}$)mol,有机物蒸气完全燃烧时需三倍于其体积的氧气,则(x+$\frac{y}{4}$-$\frac{z}{2}$)=3.
A.C2H4O分子含有2个碳原子,1mol消耗氧气为(2+$\frac{4}{4}$-0.5)mol=2.5mol,故A错误;
B.C2H5OH分子含有2个碳原子,1mol消耗氧气为(2+$\frac{6}{4}$-0.5)mol=3mol,故B正确;
C.CH3CHO分子含有2个碳原子,1mol消耗氧气为(2+1-0.5)mol=2.5mol,故C错误;
D.CH3COOH分子含有2个碳原子,1mol消耗氧气为(2+1-1)mol=2mol,故D错误,
故选:B.
点评 本题考查有机物分子式的确定,难度不大,注意根据原子守恒判断分子中碳原子数目及耗氧量规律,利用代入法验证.

练习册系列答案
相关题目
20.把下列物质分别加入盛水的锥形瓶内,立即塞紧带U 形管的塞子.已知U形管内预先装有少量水且液面相平(为便于观察,预先染成红色),加入下列( )物质后,发生如图所示变化.
①NH4NO3晶体; ②浓H2SO4; ③NaOH粉末;
④NaCl晶体 ⑤Na2O2固体; ⑥生石灰.
①NH4NO3晶体; ②浓H2SO4; ③NaOH粉末;
④NaCl晶体 ⑤Na2O2固体; ⑥生石灰.

| A. | ①②④⑤ | B. | ①②③ | C. | ③④⑤ | D. | ②③⑤⑥ |
1.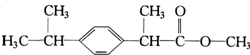 某种药物主要成分X的分子结构如图,关于有机物X的说法中错误的是( )
某种药物主要成分X的分子结构如图,关于有机物X的说法中错误的是( )
①X难溶于水,易溶于有机溶剂
②X能跟溴水反应
③X能使酸性高锰酸钾溶液褪色
④X的水解产物能发生消去反应.
 某种药物主要成分X的分子结构如图,关于有机物X的说法中错误的是( )
某种药物主要成分X的分子结构如图,关于有机物X的说法中错误的是( )①X难溶于水,易溶于有机溶剂
②X能跟溴水反应
③X能使酸性高锰酸钾溶液褪色
④X的水解产物能发生消去反应.
| A. | ①④ | B. | ②④ | C. | ②③ | D. | ①② |
14.粗CuO是将工业废铜、废电线及废铜合金高温焙烧而成的,杂质主要是铁的氧化物及泥沙,以粗CuO为原料制备CuSO4•5H2O的主要步骤如下图所示:
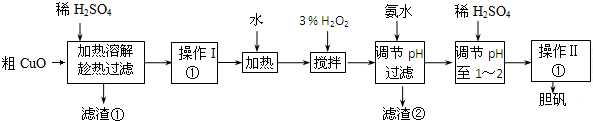
已知:Fe3+、Fe2+、Cu2+转化为氢氧化物时,开始沉淀和沉淀完全时的pH如下表:
(1)写出CuO溶解时的离子方程式CuO+2H+=Cu2++H2O.滤渣②的成分是Fe(OH)3.
(2)加入3% H2O2之前需将热溶液冷却,其目的是防止双氧水分解;加入H2O2后,发生反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)加入2mol/L氨水后,溶液的pH应在3.2~4.7范围内.
(4)经过操作Ⅰ得到粗胆矾,经过操作Ⅱ得到精制胆矾.两步操作相同,都包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥等步骤.其中“洗涤”的目的是洗去表面的杂质离子.

已知:Fe3+、Fe2+、Cu2+转化为氢氧化物时,开始沉淀和沉淀完全时的pH如下表:
| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物沉淀完全时的pH | 3.2 | 9.0 | 6.7 |
(2)加入3% H2O2之前需将热溶液冷却,其目的是防止双氧水分解;加入H2O2后,发生反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)加入2mol/L氨水后,溶液的pH应在3.2~4.7范围内.
(4)经过操作Ⅰ得到粗胆矾,经过操作Ⅱ得到精制胆矾.两步操作相同,都包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥等步骤.其中“洗涤”的目的是洗去表面的杂质离子.
1.过氧化尿素是一种新型漂白、消毒剂,广泛应用于农业、医药、日用化工等领域.湿法工艺制取过氧化尿素是用低浓度的双氧水和饱和尿素溶液在一定条件下合成过氧化尿素.反应的方程式为:CO(NH2)2+H2O2$\frac{\underline{\;30℃\;}}{\;}$CO(NH2)2•H2O2△H<0.过氧化尿素的部分性质如下:
湿法合成过氧化尿素的流程图如下:
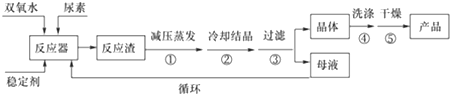
请回答下列问题:
(1)反应器的加热方式是水浴加热;反应温度需控制在适当温度下进行,温度不能过高的原因是温度过高,产品易分解,致使活性氧含量降低,温度也不能过低的原因温度过低,反应速率太慢,且反应体系制冷需要消耗大量能量.
(2)若欲从母液中分离出H2O2和尿素,可采用的操作是减压蒸馏、结晶.
(3)干法工艺制取过氧化尿素的方法是:采用高浓度双氧水水溶液喷雾到无水尿素固体上进行反应,水和反应热通过流态床移去而得到干燥的过氧化尿素产品.
比较干法与湿法两种工艺,你认为干法工艺的优点是:流程短,工艺简单 (答出一点即可),
干法工艺的缺点是:双氧水浓度高经济效益低,设备复杂;技术条件苛刻;产品稳定性差;产品污染不纯等 (答出两点即可),
湿法工艺的优点是:低浓度双氧水,经济效益高;设备简单易于达到;能耗低;产品稳定性好;母液可循环使用等 (答出两点即可).
(4)准确称取0.6000g产品于250mL锥形瓶中,加适量蒸馏水溶解,再加1mL 6mol•L-1 H2SO4,用0.1000mol•L-1 KMnO4标准溶液滴定至终点时消耗20.00mL(尿素与KMnO4溶液不反应),则产品中CO(NH2)2•H2O2的质量分数为78.3% (结果保留到小数点后一位).
| 分子式 | 外观 | 热分解温度 | 熔点 | 溶解性 |
| CO(NH2)2•H2O2 | 白色晶体 | 45℃ | 75-85℃ | 易溶于水、有机溶剂 |

请回答下列问题:
(1)反应器的加热方式是水浴加热;反应温度需控制在适当温度下进行,温度不能过高的原因是温度过高,产品易分解,致使活性氧含量降低,温度也不能过低的原因温度过低,反应速率太慢,且反应体系制冷需要消耗大量能量.
(2)若欲从母液中分离出H2O2和尿素,可采用的操作是减压蒸馏、结晶.
(3)干法工艺制取过氧化尿素的方法是:采用高浓度双氧水水溶液喷雾到无水尿素固体上进行反应,水和反应热通过流态床移去而得到干燥的过氧化尿素产品.
比较干法与湿法两种工艺,你认为干法工艺的优点是:流程短,工艺简单 (答出一点即可),
干法工艺的缺点是:双氧水浓度高经济效益低,设备复杂;技术条件苛刻;产品稳定性差;产品污染不纯等 (答出两点即可),
湿法工艺的优点是:低浓度双氧水,经济效益高;设备简单易于达到;能耗低;产品稳定性好;母液可循环使用等 (答出两点即可).
(4)准确称取0.6000g产品于250mL锥形瓶中,加适量蒸馏水溶解,再加1mL 6mol•L-1 H2SO4,用0.1000mol•L-1 KMnO4标准溶液滴定至终点时消耗20.00mL(尿素与KMnO4溶液不反应),则产品中CO(NH2)2•H2O2的质量分数为78.3% (结果保留到小数点后一位).
11.下列电离或水解方程式书写不正确的是( )
| A. | 碳酸氢钠的电离方程式为:NaHCO3═Na++HCO3- HCO3-?H++CO32- | |
| B. | 偏铝酸钠的水解方程式为:AlO2-+2H2O═Al(OH)3↓+OH- | |
| C. | 硫化铝溶于水的水解方程式为:Al2S3+6H2O═2Al(OH)3↓+3H2S↑ | |
| D. | 醋酸铵的水解方程式为:CH3COO-+NH4++H2O?CH3COOH+NH3•H2O |
18.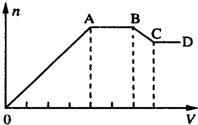 某溶液中,可能含有下表所列离子中的某几种:
某溶液中,可能含有下表所列离子中的某几种:
取少量该溶液,向其中加入某试剂X,产生沉淀的物质的量(n)与加入试剂X的体积(V)关系如图所示:
(1)若X是NaOH溶液,原溶液中一定含有的阴离子有Cl-;BC段反应的离子方程式为Al(OH)3+OH-=[Al(OH)4]-或Al(OH)3+OH-=AlO2?+H2O.
(2)若X是盐酸,则原溶液中一定含有的金属阳离子是Na+;AB段发生反应的总离子方程式为CO32-+2H+=H2O+CO2↑;OA段生成沉淀的物质的量之比为11:2.
 某溶液中,可能含有下表所列离子中的某几种:
某溶液中,可能含有下表所列离子中的某几种:| 阳离子 | Al3+、Mg2+、NH4+、Na+ |
| 阴离子 | CO32-、SiO32-、[Al(OH)4]-、Cl- |
(1)若X是NaOH溶液,原溶液中一定含有的阴离子有Cl-;BC段反应的离子方程式为Al(OH)3+OH-=[Al(OH)4]-或Al(OH)3+OH-=AlO2?+H2O.
(2)若X是盐酸,则原溶液中一定含有的金属阳离子是Na+;AB段发生反应的总离子方程式为CO32-+2H+=H2O+CO2↑;OA段生成沉淀的物质的量之比为11:2.
15.下列有关事实的叙述正确的是( )
| A. | 电解饱和NaOH溶液时溶液的pH变大 | |
| B. | 在镀件上电镀铜时,可以不用金属铜做阳极,只要溶液中存在Cu2+就可以 | |
| C. | 电解稀硫酸制O2、H2时,铜做阳极 | |
| D. | 铝-空气燃料电池通常以NaOH溶液为电解液,电池在工作过程中电解液的pH保持不变 |
16.食盐中的抗结剂是亚铁氰化钾,其化学式为K4[Fe(CN)6]•3H2O2g K4[Fe(CN)6]•3H2O(M=422g/mol)样品受热脱水过程的热重曲线(样品质量随温度的变化曲线)如图1所示.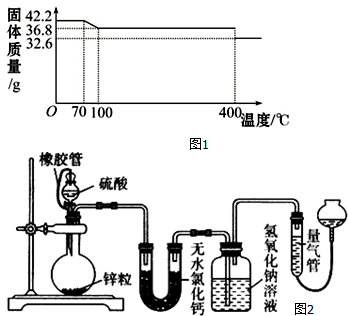
(1)试确定150℃时固体物质的化学式为K4[Fe(CN)6].
(2)在25℃下,将a mol•L-1的KCN(pH>7)溶液与0.01mol•L-1的盐酸等体积混合,反应平衡时,测得溶液pH=7,则KCN溶液的物质的量浓度a>0.01mol•L-1(填“>”、“<”或“=”);用含a的代数式表示HCN的电离常数Ka=(100a-1)×10-7 mol•L-1.
(3)在Fe2+、Fe3+的催化作用下,可实现2SO2+O2+2H2O═2H2SO4的转化.已知,含SO2的废气通入Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2++O2+4H+═4Fe3++2H2O,则另一反应的离子方程式为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+.
(4)不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气.为了验证这一事实,某同学拟用如图2装置进行实验(实验时压强为10lkPa,温度为0℃).
(Ⅰ)若在烧瓶中投入d g锌,加入一定量的c mol/L 浓硫酸V L,充分反应后锌有剩余,测得氢氧化钠洗气瓶增重mg,则整个实验过程产生的气体中n(H2)=(cV-$\frac{m}{32}$)mol(用含字母的代数式表示).若撤走盛有无水氯化钙的U型管,n(SO2):n(H2)的数值将偏大(填偏大、偏小或无影响)
(Ⅱ)在硫酸中加入硫酸铜可以加快氢气的生成速率的原因:锌和铜构成原电池,加快反应速率
(Ⅲ)为进一步探究硫酸铜的量对氢气生成速率的影响,某同学设计如下一系列实验,将表中所给的混合溶液分别加入到5个盛有过量Zn粒的反应瓶中.
①完成此实验设计,其中V5=5,V7=9
②为探究氢气生成速率要收集产生的气体,还需记录:收集等体积气体所需时间.

(1)试确定150℃时固体物质的化学式为K4[Fe(CN)6].
(2)在25℃下,将a mol•L-1的KCN(pH>7)溶液与0.01mol•L-1的盐酸等体积混合,反应平衡时,测得溶液pH=7,则KCN溶液的物质的量浓度a>0.01mol•L-1(填“>”、“<”或“=”);用含a的代数式表示HCN的电离常数Ka=(100a-1)×10-7 mol•L-1.
(3)在Fe2+、Fe3+的催化作用下,可实现2SO2+O2+2H2O═2H2SO4的转化.已知,含SO2的废气通入Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2++O2+4H+═4Fe3++2H2O,则另一反应的离子方程式为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+.
(4)不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气.为了验证这一事实,某同学拟用如图2装置进行实验(实验时压强为10lkPa,温度为0℃).
(Ⅰ)若在烧瓶中投入d g锌,加入一定量的c mol/L 浓硫酸V L,充分反应后锌有剩余,测得氢氧化钠洗气瓶增重mg,则整个实验过程产生的气体中n(H2)=(cV-$\frac{m}{32}$)mol(用含字母的代数式表示).若撤走盛有无水氯化钙的U型管,n(SO2):n(H2)的数值将偏大(填偏大、偏小或无影响)
(Ⅱ)在硫酸中加入硫酸铜可以加快氢气的生成速率的原因:锌和铜构成原电池,加快反应速率
(Ⅲ)为进一步探究硫酸铜的量对氢气生成速率的影响,某同学设计如下一系列实验,将表中所给的混合溶液分别加入到5个盛有过量Zn粒的反应瓶中.
| 实验 溶液 | A | B | C | D | E |
| 5mol/LH2SO4 mL | 40 | V1 | V2 | V3 | V4 |
| 饱和CuSO4液 mL | 0 | 1 | 2 | V5 | 10 |
| H2O mL | V6 | V7 | V8 | 5 | 0 |
②为探究氢气生成速率要收集产生的气体,还需记录:收集等体积气体所需时间.