题目内容
17.下列物质性质的比较,不能用元素周期律解释的是( )| A. | 稳定性:H2O>NH3 | B. | 碱性:NaOH>Al(OH)3 | ||
| C. | 氧化性:F2>Cl2 | D. | 酸性:CH3COOH>H2CO3 |
分析 A.非金属性越强,氢化物越稳定;
B.金属性越强,最高价氧化物的水化物碱性越强;
C.非金属性越强,对应单质的氧化性越强;
D.由醋酸可与碳酸钙反应生成碳酸判断酸性.
解答 解:A.非金属性O>N,稳定性:H2O>NH3,故A正确;
B.金属性Na>Al,最高价氧化物的水化物碱性为NaOH>Al(OH)3,故B正确;
C.非金属性F>Cl,对应单质的氧化性为F2>Cl2,故C正确;
D.由醋酸可与碳酸钙反应生成碳酸判断酸性CH3COOH>H2CO3,不能利用元素周期律解释,故D错误;
故选D.
点评 本题考查性质及解释,为高频考点,把握元素周期表和周期律、强酸制取弱酸的反应原理为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
7.下列离子在溶液中能大量共存的是( )
| A. | H+、I-、NO3-、SiO32- | B. | Ag+、Fe3+、Cl-、SO42- | ||
| C. | K+、SO42-、Cu2+、NO3- | D. | NH4+、OH-、Cl-、HCO3- |
8.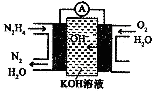 肼(N2H4)又称联氨,广泛用于火箭推进剂、化工原料及燃料电池等方面.请回答下列问题:
肼(N2H4)又称联氨,广泛用于火箭推进剂、化工原料及燃料电池等方面.请回答下列问题:
(1)肼是火箭的高能燃料,该物质燃烧时生成水蒸气和氮气,已知某些化学键能如下:
①N2H4中氮元素的化合价为-2.
②气态N2H4在氧气中燃烧的热化学方程式为N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=一591kJ/mol.
(2)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液,该反应的离子方程式为ClO-+2NH3=N2H4+Cl-+H2O.
(3)肼燃料电池原理如图所示,左边电极上发生反应的电极反应式为:N2H4-4e-+4OH-=N2+4H2O.
(4)盐酸肼(N2H6Cl2)是一种化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4 Cl类似,但分步水解.
①写出盐酸肼第一步水解的离子方程式N2H62++H2O═[N2H5•H2O]++H+.
②盐酸肼水溶液中离子浓度的关系为B (填序号).
A.c(Cl-)>c([N2H5•H2O+])>c(H+)>c(OH-)
B.c(Cl-)>c(N2H62+)>c(H+)>c(OH-)
C. c(N2H62+)+c([N2H5•H2O+])+c(H+)=c(Cl-)+c(OH-)
(5〕常温下,将0.2mol/L盐酸与0.2mol/L肼的溶液等体积混合(忽略混合后溶液体积变化〕.若测定混合液的pH=6,混合液中水电离出的H+与0.1mol/L盐酸中水电离出的H+浓度之比为107:1.
 肼(N2H4)又称联氨,广泛用于火箭推进剂、化工原料及燃料电池等方面.请回答下列问题:
肼(N2H4)又称联氨,广泛用于火箭推进剂、化工原料及燃料电池等方面.请回答下列问题:(1)肼是火箭的高能燃料,该物质燃烧时生成水蒸气和氮气,已知某些化学键能如下:
| 化学键 | O-H | N-N | N-H | O=O | N═N |
| 键能/KJ•mol-1 | 467 | 160 | 391 | 498 | 945 |
②气态N2H4在氧气中燃烧的热化学方程式为N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=一591kJ/mol.
(2)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液,该反应的离子方程式为ClO-+2NH3=N2H4+Cl-+H2O.
(3)肼燃料电池原理如图所示,左边电极上发生反应的电极反应式为:N2H4-4e-+4OH-=N2+4H2O.
(4)盐酸肼(N2H6Cl2)是一种化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4 Cl类似,但分步水解.
①写出盐酸肼第一步水解的离子方程式N2H62++H2O═[N2H5•H2O]++H+.
②盐酸肼水溶液中离子浓度的关系为B (填序号).
A.c(Cl-)>c([N2H5•H2O+])>c(H+)>c(OH-)
B.c(Cl-)>c(N2H62+)>c(H+)>c(OH-)
C. c(N2H62+)+c([N2H5•H2O+])+c(H+)=c(Cl-)+c(OH-)
(5〕常温下,将0.2mol/L盐酸与0.2mol/L肼的溶液等体积混合(忽略混合后溶液体积变化〕.若测定混合液的pH=6,混合液中水电离出的H+与0.1mol/L盐酸中水电离出的H+浓度之比为107:1.
5.对下列两种有机物的描述正确的是( )


| A. | 苯环上的一氯代物种数相同 | |
| B. | 分子中共面的碳原子数一定相同 | |
| C. | 1 mol甲与浓溴水反应最多能消耗4 mol Br2 | |
| D. | 甲、乙可用红外光谱区分,但不能用核磁共振氢谱区分 |
12. 如图是一种应用广泛的锂电池,LiPF6是电解质,SO(CH3)2是溶剂,反应原理是4Li+FeS2═Fe+2Li2S.下列说法正确的是( )
如图是一种应用广泛的锂电池,LiPF6是电解质,SO(CH3)2是溶剂,反应原理是4Li+FeS2═Fe+2Li2S.下列说法正确的是( )
 如图是一种应用广泛的锂电池,LiPF6是电解质,SO(CH3)2是溶剂,反应原理是4Li+FeS2═Fe+2Li2S.下列说法正确的是( )
如图是一种应用广泛的锂电池,LiPF6是电解质,SO(CH3)2是溶剂,反应原理是4Li+FeS2═Fe+2Li2S.下列说法正确的是( )| A. | Li 发生氧化反应,a 极为阴极 | |
| B. | 电子由 a 极流出通过电流表流入 b 极,然后再由 b 极经内电路回到 a 极 | |
| C. | 可以用水代替 SO(CH3)2做溶剂 | |
| D. | b 极反应式是 FeS2+4Li++4e-═Fe+2Li2S |
9.食盐中含有一定量的镁、铁等杂质,加碘盐中碘的损失主要是由于杂质、水分、空气中的氧气以及光照、受热而引起的.
已知:①氧化性:IO3->Fe3+>I2;还原性:S2O32->I-;②KI+I2?KI3
(1)某学习小组对加碘盐进行如下实验:取一定量某加碘盐(可能含有KIO3、KI、Mg2+、Fe2+、Fe3+),用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分为4份.第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显淡黄色,用CCl4萃取,下层溶液显紫红色;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色.
①向第四份试液中加K3Fe(CN)6溶液,根据是否得到具有特征蓝色的沉淀,可检验是否含有Fe2+(用离子符号表示).
②第二份试液中加入足量KI固体后,反应的离子方程式为:IO3-+5I-+6H+=3I2+3H2O、2Fe3++2I-=2Fe2++I2.
(2)KI作为加碘剂的食盐在保存过程中,由于空气中氧气的作用,容易引起碘的损失写出潮湿环境下KI与氧气反应的化学方程式:O2+4KI+2H2O=2I2+4KOH.
将I2溶于KI溶液,在低温条件下,可制得KI3•H2O.该物质不适合作为食盐加碘剂,其理由是KI3在受热(或潮湿)条件下产生I2和KI,KI被氧气氧化,I2易升华.
(3)某同学为探究温度和反应物浓度对反应2IO3-+5SO32-+2H+=I2+5SO42-+H2O的速率的影响,设计实验如下表所示:
表中数据:t1<t2(填“>”、“<”或“=”);表中V2=40mL.
已知:①氧化性:IO3->Fe3+>I2;还原性:S2O32->I-;②KI+I2?KI3
(1)某学习小组对加碘盐进行如下实验:取一定量某加碘盐(可能含有KIO3、KI、Mg2+、Fe2+、Fe3+),用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分为4份.第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显淡黄色,用CCl4萃取,下层溶液显紫红色;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色.
①向第四份试液中加K3Fe(CN)6溶液,根据是否得到具有特征蓝色的沉淀,可检验是否含有Fe2+(用离子符号表示).
②第二份试液中加入足量KI固体后,反应的离子方程式为:IO3-+5I-+6H+=3I2+3H2O、2Fe3++2I-=2Fe2++I2.
(2)KI作为加碘剂的食盐在保存过程中,由于空气中氧气的作用,容易引起碘的损失写出潮湿环境下KI与氧气反应的化学方程式:O2+4KI+2H2O=2I2+4KOH.
将I2溶于KI溶液,在低温条件下,可制得KI3•H2O.该物质不适合作为食盐加碘剂,其理由是KI3在受热(或潮湿)条件下产生I2和KI,KI被氧气氧化,I2易升华.
(3)某同学为探究温度和反应物浓度对反应2IO3-+5SO32-+2H+=I2+5SO42-+H2O的速率的影响,设计实验如下表所示:
| 0.01mol•L-1KIO3 酸性溶液(含淀粉) 的体积/mL | 0.01mol•L-Na2SO3 溶液的体积/mL | H2O的 体积/mL | 实验 温度 /℃ | 溶液出现 蓝色时所 需时间/s | |
| 实验1 | 5 | V1 | 35 | 25 | t1 |
| 实验2 | 5 | 5 | 40 | 25 | t2 |
| 实验3 | 5 | 5 | V2 | 0 | t3 |
6.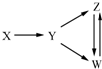 一定条件下,下列各组物质能一步实现图所示转化关系的是( )
一定条件下,下列各组物质能一步实现图所示转化关系的是( )
 一定条件下,下列各组物质能一步实现图所示转化关系的是( )
一定条件下,下列各组物质能一步实现图所示转化关系的是( )| 选项 | X | Y | Z | W |
| A | Al | Al2O3 | NaAlO2 | Al(OH)3 |
| B | Fe3O4 | Fe | FeCl2 | FeCl3 |
| C | H2SO4 | SO2 | S | SO3 |
| D | CH3CH2Br | CH2═CH2 | C2H5OH | CH2BrCH2Br |
| A. | A | B. | B | C. | C | D. | D |
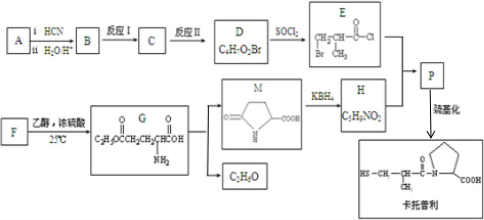
 (R1、R2为烃基)
(R1、R2为烃基)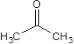 .
. ,反应Ⅱ所用试剂是HBr.
,反应Ⅱ所用试剂是HBr. .
.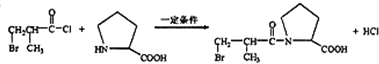 .
. (任写一种).
(任写一种).