题目内容
12.据报道,科学家已成功合成了H3,下列说法正确的是( )| A. | H3的摩尔质量是3g | |
| B. | H3是氢元素的一种新的同位素 | |
| C. | H3分子中含有3个中子 | |
| D. | H2和H3是氢元素形成的两种不同单质 |
分析 A.摩尔质量的单位是g/mol;
B.同位素是质子数相同中子数不同的一类原子;
C.H3分子由3个氢原子核(只有质子)和3个电子构成;
D.H2和H3是单质.
解答 解:A.H3的摩尔质量是3 g•mol-1,故A错误;
B.H3是氢元素的一种单质,故B错误;
C.H3分子由3个氢原子核(只有质子)和3个电子构成,不含中子,故C错误;
D.H2和H3是两种不同单质,故D正确.
故选D.
点评 本题考查了物质中含有粒子数目的计算、同位素、同素异形体等知识点,难度不大,明确同位素和同素异形体的区别.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.下列物质中属于弱电解质的是( )
| A. | 氨水 | B. | 盐酸 | C. | 碳酸氢钠 | D. | 冰醋酸 |
20.在0.1mol•L-1氨水中存在如下电离平衡:NH3•H2O?NH4++OH-,对于该平衡,下列叙述正确的是( )
| A. | 加入水时,溶液中c(OH-) 增大 | |
| B. | 加入少量NH4Cl固体,平衡向逆方向移动,电离平衡常数减小 | |
| C. | 通入少量HCl气体,溶液中c(NH4+)增大 | |
| D. | 降低温度,促进NH3•H2O电离 |
17.人们对原子结构的认识有一个不断深入的过程,下列先后顺序中符合史实的是( )
①道尔顿提出的原子论②卢瑟福的原子结构行星模型③玻尔提出的原子力学模型④汤姆孙提出的葡萄干面包原子模型.
①道尔顿提出的原子论②卢瑟福的原子结构行星模型③玻尔提出的原子力学模型④汤姆孙提出的葡萄干面包原子模型.
| A. | ①②③④ | B. | ①③②④ | C. | ②①④③ | D. | ①④②③ |
4.鉴别NaCl、NaBr、NaI可以采用的试剂是( )
| A. | 碘水、淀粉溶液 | B. | 碘化钾淀粉溶液 | C. | 氯水、CCl4 | D. | 溴水、汽油 |
1.下列有关电解质溶液中粒子的物质的量浓度大小关系正确的是( )
| A. | 等物质的量浓度的下列溶液:①H2CO3 ②Na2CO3 ③NaHCO3 ④(NH4)2CO3其中c(CO32-)的大小关系为:②>④>③>① | |
| B. | pH=2的H2C2O4溶液与pH=12的NaOH溶液等体积混合:c(Na+)+c(H+)=c(OH-)+c( HC2O4-)+c( C2O42-) | |
| C. | 向0.2 mol•L-1NaHCO3溶液中加入等体积0.1 mol•L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) | |
| D. | 常温下,同浓度的CH3COONa与CH3COOH溶液等体积混合,溶液的pH<7:c(CH3COOH)+c(OH-)>c(Na+)+c(H+) |
 300℃下,将2mol SO21mol O2混合于2L的恒容密闭容器中,发生反应:2SO2(g)+O2(g)?2SO3(g)△H,2分钟末达到平衡,测得SO2的转化率为60%,请根据化学反应的有关原理回答下列问题:
300℃下,将2mol SO21mol O2混合于2L的恒容密闭容器中,发生反应:2SO2(g)+O2(g)?2SO3(g)△H,2分钟末达到平衡,测得SO2的转化率为60%,请根据化学反应的有关原理回答下列问题: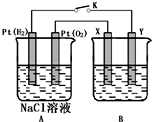 某化学兴趣小组用下图所示装置进行电化学原理的实验探究,回答下列问题:
某化学兴趣小组用下图所示装置进行电化学原理的实验探究,回答下列问题: