题目内容
1.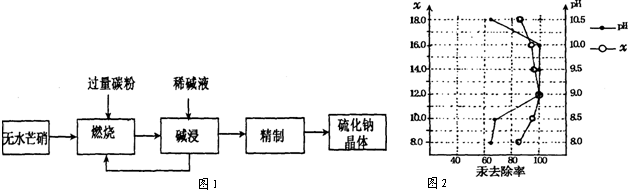
工业生产Na2S常用方法是:无水芒硝(Na2SO4)一碳还原法,其流程示意图如图1.
(1)若煅烧阶段所得气体为等物质的量CO和CO2.写出煅烧时发生的总反应方程式:3Na2SO4+8C$\frac{\underline{\;\;△\;\;}}{\;}$3Na2S+4CO2↑+4CO↑;
(2)用碱液浸出产品比用热水更好,理由是:热水能促进Na2S水解,而稀碱可抑制Na2S水解;
(3)废水中汞常用硫化钠除去,汞的除去率与溶液pH和硫化钠实际用量与理论用量比值X的关系如图2所示.为使除汞达到最佳效果,应控制条件是pH介于9~10之间,x=12.
(4)取Na2S(含少量NaOH),加人到CuSO4溶液中,充分搅拌,若反应后溶液pH=4,此时溶液中c(S 2-)=4.0×10-36 mol/L;(保留2位有效数字)(已知:CuS Ksp=8.8×10-36;Cu(OH)2 Ksp=2.2×10-20)
(5)纳米Cu2O常用电解法制备,制备过程用铜棒和石墨棒作电极,Cu(NO3)2作电解液.电解生成Cu2O应在阴极;该电极pH将降低(填“升高”,“不变”或“降低”),用电极方程式解释pH发生变化的原因:2Cu2++2e-+H2O=Cu2O↓+2H+.
分析 根据图1可知,制备硫化钠晶体的流程为:无水芒硝(Na2SO4)与碳在高温煅烧反应:3Na2SO4+8C$\frac{\underline{\;\;△\;\;}}{\;}$3Na2S+4CO2↑+4CO↑,由于硫离子水解,则用稀碱溶液浸泡抑制硫离子水解,通过精制获得硫化钠晶体,
(1)煅烧中得到等物质的量的CO和CO2,S元素被还原得到Na2S;
(2)热水促进硫化钠水解,用碱液抑制硫化钠水解;
(3)硫化钠实际用量与理论用量比值x越小、汞除去率越高,最佳效果;
(4)根据Cu(OH)2溶度积可求得c(Cu2+),代入CuS的溶度积求得c(S2-);
(5)Cu由+2价变为+1价,得电子,在阴极生成,反应式为:2Cu2++2e-+H2O=Cu2O↓+2H+.
解答 解:(1)煅烧中得到等物质的量的CO和CO2,S元素被还原得到Na2S,反应方程式为3Na2SO4+8C$\frac{\underline{\;\;△\;\;}}{\;}$3Na2S+4CO2↑+4CO↑;
故答案为:3Na2SO4+8C$\frac{\underline{\;\;△\;\;}}{\;}$3Na2S+4CO2↑+4CO↑;
(2)Na2S是强碱弱酸盐,水解后溶液显碱性,加热会促进S2-水解,而加碱则可以抑制其水解;
故答案为:热水能促进Na2S水解,而稀碱可抑制Na2S水解;
(3)硫化钠实际用量与理论用量比值x越小、汞除去率越高,最佳效果,由图象可知当pH介于9~10时,x=12时汞的除去率最大;
故答案为:pH介于9~10之间,x=12;
(4)溶液pH=4,则溶液中c(OH-)=10-10 mol/L,根据Cu(OH)2溶度积可得c(Cu2+)=$\frac{2.2×1{0}^{-20}}{(1{0}^{-10})^{2}}$mol/L=2.2 mol/L,代入CuS的溶度积可得c(S2-)=$\frac{8.8×1{0}^{-36}}{2.2}$mol/L=4.0×10-36 mol/L;
故答案为:4.0×10-36 mol/L;
(5)电解生成Cu2O,Cu元素由+2价变为+1价,得电子,发生还原反应,则Cu2O在阴极生成,发生电极反应式为:2Cu2++2e-+H2O=Cu2O↓+2H+,由于反应中有H+生成,所以溶液的pH降低;
故答案为:阴极;降低;2Cu2++2e-+H2O=Cu2O↓+2H+.
点评 本题是对化学与技术的考查,涉及常见化学工业、对操作的分析评价、对条件的控制、溶度积计算、电解原理等,侧重考查学生理论联系实际的能力、阅读获取信息的能力、知识迁移应用,难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | H2O>H2S | B. | NaCl>O2 | C. | Na>K | D. | SiO2>CO2 |
| A. | 硫酸型酸雨的形成涉及反应:2H2SO3+O2$\frac{\underline{\;催化剂\;}}{\;}$2H2SO4 | |
| B. | SO2的水溶液显酸性:SO2+H2O?H2SO3?2H++SO32- | |
| C. | 常温下,0.1mol/L醋酸溶液pH≈3:CH3COOH?CH3COO-+H+ | |
| D. | Mg(OH)2固体在溶液中存在平衡:Mg(OH)2(s)?Mg2+(aq)+2OH-(aq),该固体可溶于NH4Cl溶液 |
| A. | 同质量的气体A与气体B,所含分子数目之比为a:b | |
| B. | 气体A与气体B的摩尔质量之比为a:b | |
| C. | 相同条件下,a g气体A与b g气体B体积之比为b:a | |
| D. | 相同条件下,气体A与气体B的密度之比为b:a |
| A. | 做“钠与水的反应”实验时.切取绿豆大小的金属钠,用滤纸吸干表面煤油,放入烧杯中,滴入两滴酚酞溶液,再加入少量水,然后观察并记录实验现象 | |
| B. | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置;下层液体显紫红色;则氧化性:Fe3+>I2 | |
| C. | 测定等浓度的Na2CO3和Na2SO3 溶液的pH;前者pH 比后者的大;则非金属性:S>C | |
| D. | 溴乙烷与 NaOH 溶液共热后,加入AgNO3溶液;未出现淡黄色沉淀;说明溴乙烷没有水解 |
 肼(N2H4)和氨是氮的两种常见化合物,在科学技术和生产中有广泛应用.回答下列问题:
肼(N2H4)和氨是氮的两种常见化合物,在科学技术和生产中有广泛应用.回答下列问题:(1)N2H4中N原子核外最外层达到8电子稳定结构.写出N2H4的结构式:
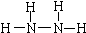 .
.(2)实验室用两种固体制取NH3的反应化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.
(3)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为2NH3+NaClO=N2H4+NaCl+H2O.
(4)肼一空气燃料电池是一种碱性环保电池,该电池放电时,负极的反应式为N2H4+4OH--4e-=N2+4H2O.
(5)工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2]反应的化学方程式为2NH3(g)+CO2(g)?CO(NH2)2(l)+H2O(l),该反应的平衡常数和温度关系如表:
| T/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
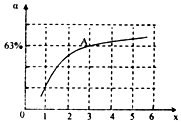
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)[n(NH3):n(CO2]=x,如图是氨碳比(x)与CO2平衡转化率(α)的关系.α随着x增大而增大的原因是c(NH3)增大,平衡正向移动.图中A点处,NH3的平衡转化率为42%.
| n(N2) | n(H2) | n(NH3) | |
| 甲 | 1mol | 3mol | 0mol |
| 乙 | 0.5mol | 1.5mol | 1mol |
| 丙 | 0mol | 0mol | 4mol |
①判断乙容器中反应进行的方向是逆向(填“正向或“逆向”)移动.
②达平衡时,甲、乙、丙三容器中NH3的体积分数大小顺序为丙>甲=乙.
(7)氨气在纯氧中燃烧,生成一种单质和水,试写出该反应的化学方程式:4NH3+5O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O,科学家利用此原理,设计成氨气一氧气燃料电池,则通入氨气的电极是负极 (填“正极”或“负极”);碱性条件下,该电极发生反应的电极反应式为2NH3-6e-+6OH-=N2+6H2O.
(8)一定条件下,某密闭容器中发生反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g).在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是c(填字母代号).
a.增大压强 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂
(9)如果某氨水的电离程度为1%,浓度为0.01mol/LMgCl2溶液滴加氨水至开始产生沉淀时(不考虑溶液体积变化),溶液中的NH3•H2O的浓度为0.002mol/L[已知Ksp[Mg(OH)2]=4.0×10-12].
| A. | 常温常压下,44 g C3H8中含有的碳碳单键数为3NA | |
| B. | 标准状况下,22.4L 甲醇中含有的氧原子数为1NA | |
| C. | 1mol羟基中电子数为10NA | |
| D. | 在30 g甲醛和醋酸的混合物中,含有碳原子数为1NA |
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
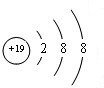
(2)①~⑩元素的最高价氧化物对就的水化物中酸性最强的是HClO4,碱性最强的是KOH;
(3)按要求写出下列两种物质的电子式:①的氢化物
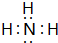 ;⑨的最高价氧化物对应的水化物
;⑨的最高价氧化物对应的水化物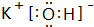 ;
;(4)在⑦与⑩的单质中,化学性质较活泼的是Cl2,可用1个化学反应说明该事实(写出反应的化学方程式):Cl2+2KBr═2KCl+Br2.