题目内容
10.很多电解过程都会产生氢气.(1)在 25℃时,用石墨电极电解一定量的饱和 Na2CO3溶液,则阴极的电极反应式为2H++2e-=H2↑或2H2O+2e-=H2↑+2OH-,阳极电极反应式为4OH--4e-=O2↑+2H2O或2H2O-4e-=O2↑+4H+,溶液 pH不变(填增大,减小或不变)
(2)电解法制取 Na2FeO4,同时可获得氢气:Fe+2H2O+2OH- $\frac{\underline{\;通电\;}}{\;}$FeO42-+3H2↑,工作原理如图1所示.装置通电后,铁电极附近生成紫红色的 FeO42-,镍电极有气泡产生.若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质.已知:Na2FeO4只在强碱性条件下稳定,易被H2还原.
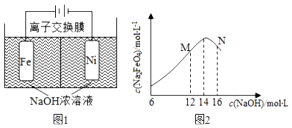
①阳极电极反应式Fe-6e-+8OH-=FeO42-+4H2O,电解一段时间后,c(OH-)降低的区域在阳极室(填“阴极室”或“阳极室”).
②电解过程中,须将阴极产生的气体及时排出,其原因是防止Na2FeO4与H2反应使产率降低.
③c( Na2FeO4)随初始 c(NaOH)的变化如图 2,分析 N 点 c( Na2FeO4)低于最高值的原因N点:c(OH-)过高,铁电极上有氢氧化铁生成,使Na2FeO4产率降低.
分析 (1)分析碳酸钠溶液中含有阳离子、阴离子,依据放电顺序判断放电离子写出电极反应式,依据电极反应式判断溶液pH变化;
(2)①电解池中阳极发生氧化反应,依据题意可知铁在阳极失去电子,碱性环境下生成高铁酸根离子,据此书写电极反应式;根据题意镍电极有气泡产生是氢离子放电生成氢气,铁电极发生氧化反应,溶液中的氢氧根离子减少;
②氢气具有还原性,根据题意Na2FeO4只在强碱性条件下稳定,易被H2还原.电解过程中,须将阴极产生的气体及时排出,防止Na2FeO4与H2反应使产率降低;
③根据题意Na2FeO4只在强碱性条件下稳定,在M点,c(OH-)低,Na2FeO4稳定性差,且反应慢,在N点:c(OH-)过高,铁电极上有氢氧化铁生成,使Na2FeO4产率降低.
解答 解:(1)碳酸钠溶液中含有阳离子为钠离子与氢离子,氢离子还原性强于钠离子,所以阴极电极反应为:
2H++2e-=H2↑ 或2H2O+2e-=H2↑+2OH-;碳酸钠溶液中含有阴离子为碳酸根离子、氢氧根离子,依据放电顺序可知氢氧根离子在阳极失去电子发生氧化反应,电极反应式为:4OH--4e-=O2↑+2H2O或2H2O-4e-=O2↑+4H+,所以电解实质为电解水,溶液为饱和碳酸钠溶液,电解过程中溶液浓度不变,溶液pH不变;
故答案为:2H++2e-=H2↑ 或2H2O+2e-=H2↑+2OH-;4OH--4e-=O2↑+2H2O或2H2O-4e-=O2↑+4H+; 不变;
(2)①电解池中阳极发生氧化反应,依据题意可知铁在阳极失去电子,碱性环境下生成高铁酸根离子,电极反应式为:Fe-6e-+8OH-=FeO42-+4H2O;
根据题意镍电极有气泡产生是氢离子放电生成氢气,铁电极发生氧化反应,溶液中的氢氧根离子减少,因此电解一段时间后,c(OH-)降低的区域在阳极室;
故答案为:Fe-6e-+8OH-=FeO42-+4H2O; 阳极室;
②氢气具有还原性,根据题意Na2FeO4只在强碱性条件下稳定,易被H2还原.电解过程中,须将阴极产生的气体及时排出,防止Na2FeO4与H2反应使产率降低,
故答案为:防止Na2FeO4与H2反应使产率降低;
③根据题意Na2FeO4只在强碱性条件下稳定,在M点,c(OH-)低,Na2FeO4稳定性差,且反应慢,在N点:c(OH-)过高,铁电极上有氢氧化铁生成,使Na2FeO4产率降低;
故答案为:N点:c(OH-)过高,铁电极上有氢氧化铁生成,使Na2FeO4产率降低.
点评 本题为电化学试题,考查了电解法制取 Na2FeO4,明确电解池工作原理及电极反应式的书写方法是解题关键,题目难度中等.

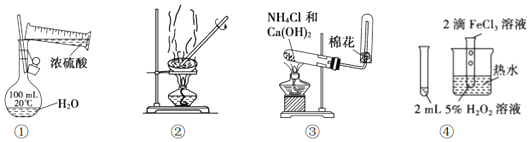
| A. | 用装置①配制一定浓度的硫酸溶液 | |
| B. | 用装置②分离溶解在CCl4中的 I2 | |
| C. | 用装置③制备和收集少量 NH3 | |
| D. | 用装置④验证FeCl3对 H2O2分解有催化作用 |
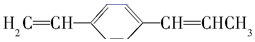 的说法正确的是( )
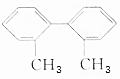
的说法正确的是( )| A. | 所有原子都在同一平面上 | |
| B. | 最多有4个碳原子在同一直线上 | |
| C. | 有7个碳原子可能在同一直线上 | |
| D. | 最多只能有9个碳原子在同一平面上 |
| A. | 乙烯通入溴的四氯化碳溶液中,溶液褪色 | |
| B. | 光照甲烷和氯气的混合气体后,瓶壁上有油状液滴附着 | |
| C. | 苯滴加到溴水中,震荡后水层接近无色 | |
| D. | 在葡萄糖溶液中加入新制的氢氧化铜,加热后产生砖红色沉淀 |
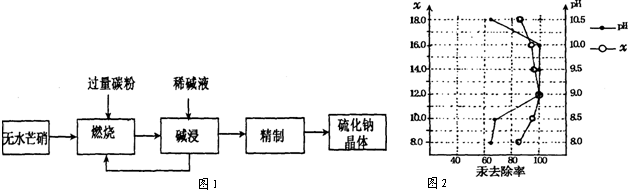
 ,请完成下列空白:
,请完成下列空白: