题目内容
6.在原子序数为1~18号的元素中,将形成的相应的物质填入下列空格中:(填元素符号或化学式)(1)与水反应最剧烈的金属是Na;
(2)原子半径最小的元素是H;
(3)常温下既能溶于强酸又能溶于强碱的氧化物是Al2O3;
(4)气态氢化物最稳定的是HF;
(5)最高价氧化物对应的水化物碱性最强的碱是NaOH.
分析 (1)同周期自左而右金属性减弱,同主族自上而下金属性增强,金属性越强,金属与水反应越剧烈;
(2)同周期自左而右原子半径减小,同主族自上而下原子半径增大,所有元素中H原子半径最小;
(3)氧化铝属于两性氧化物,能溶于强酸又能溶于强碱;
(4)同周期自左而右非金属性增强,同主族自上而下非金属性减弱,非金属性越强,对应氢化物越稳定;
(5)金属性越强,最高价氧化物对应水化物的碱性越强.
解答 解:(1)同周期自左而右金属性减弱,同主族自上而下金属性增强,Na的金属性最强,与水反应最最剧烈,故答案为:Na;
(2)同周期自左而右原子半径减小,同主族自上而下原子半径增大,所有元素中H原子半径最小,故答案为:H;
(3)Al2O3属于两性氧化物,能溶于强酸又能溶于强碱,故答案为:Al2O3;
(4)同周期自左而右非金属性增强,同主族自上而下非金属性减弱,F元素非金属性最强,非金属性越强,对应氢化物越稳定,故HF最稳定,故答案为:HF;
(5)Na的金属性最强,金属性越强,最高价氧化物对应水化物的碱性越强,故NaOH碱性最强,故答案为:NaOH.
点评 本题考查元素周期表与元素周期律,侧重对元素周期律的考查,注意对元素周期律的理解掌握,有利于基础知识的巩固.

练习册系列答案
相关题目
11.表中是食用碘盐包装上的部分说明,下列说法正确的是( )
| 配料 | 精盐、碘酸钾(KIO3)、抗结剂 |
| 碘含量 | 35±15mg/kg |
| 储存方法 | 密封、避光、防潮 |
| 食用方法 | 烹饪时,待食品熟后加入碘盐 |
| A. | 高温会导致碘的损失 | B. | 碘酸钾可氧化氯化钠 | ||
| C. | 可用淀粉检验碘盐中的碘酸钾 | D. | 该碘盐中碘含量是指碘酸钾的含量 |
17.50mL 1mol/L氯化铝溶液中c(Cl-)相等的是( )
| A. | 150ml 1mol/L氯化钠溶液 | B. | 150ml 3mol/L氯化钾溶液 | ||
| C. | 75ml 2mol/L氯化铵溶液 | D. | 50ml 1mol/L氯化钡溶液 |
1.如图是元素周期表的一部分
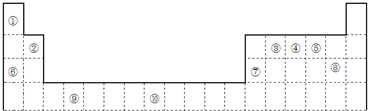
(1)元素⑩的次外层电子数为14个.
(2)如果在温度接近373K时,根据M=m/n测定⑤的气态氢化物的相对分子质量,结果发现测定结果比理论值高,其原因是分子间存在氢键,H2O分子发生缔合;
(3)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的氢氧化物有相似的性质.写出元素②的氢氧化物与NaOH溶液反应的离子方程式2OH-+Be(OH)2=BeO22-+2H2O;
(4)根据下列五种元素的第一至第四电离能数据(单位:kJ•mol-1),回答下面各题:
①在周期表中,最可能处于同一主族的是R和U.(填元素代号)
②T元素最可能是p(填“s”、“p”、“d”、“ds”等)区元素;若T为第二周期元素,Z是第三周期元素中原子半径最小的主族元素,则T、Z形成的化合物分子键角为120°.

(1)元素⑩的次外层电子数为14个.
(2)如果在温度接近373K时,根据M=m/n测定⑤的气态氢化物的相对分子质量,结果发现测定结果比理论值高,其原因是分子间存在氢键,H2O分子发生缔合;
(3)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的氢氧化物有相似的性质.写出元素②的氢氧化物与NaOH溶液反应的离子方程式2OH-+Be(OH)2=BeO22-+2H2O;
(4)根据下列五种元素的第一至第四电离能数据(单位:kJ•mol-1),回答下面各题:
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
②T元素最可能是p(填“s”、“p”、“d”、“ds”等)区元素;若T为第二周期元素,Z是第三周期元素中原子半径最小的主族元素,则T、Z形成的化合物分子键角为120°.
11.下列分子式表示的物质一定是纯净物的是( )
| A. | C5H10 | B. | C4H8 | C. | C2H4 | D. | C2H4Cl2 |
18.科学家在《Science》上发表论文,宣布发现了铝的超原子结构Al13和Al14,Al13、Al14的性质很像现行周期表中的某主族元素,当这类超原子具有40个价电子(对于主族元素的原子,外围电子又称为价电子)时最稳定,在质谱仪上可检测到稳定到Al13-和Al142+.下列说法错误的是( )
| A. | Al14和稀盐酸反应的化学方程式可表示为Al14+2HCl→Al14Cl2+H2↑ | |
| B. | Al13超原子中Al原子间是通过共价键结合的 | |
| C. | Al14、Al13性质与Al相似,都具有较强的还原性 | |
| D. | Al13和Al14互为同位素 |
15.下列溶液的溶质都是强电解质,这些溶液中的Cl?浓度与50mL 1mol•L-1 MgCl2溶液中的Cl-浓度相等的是( )
| A. | 150mL 1mol•L-1NaCl溶液 | B. | 75mL 1mol•L-1 CaCl2溶液 | ||
| C. | 150mL 1mol•L-1 KCl溶液 | D. | 75mL 1mol•L-1 AlCl3溶液 |
16.常温下,下列离子浓度大小比较正确的是( )
| A. | pH=4的NaHSO3溶液中:c(Na+)>c(H+)>c(HSO3-)>c(SO32-)>C(OH-) | |
| B. | 0.2mol•L-1Na2CO3溶液和0.1mol•L-1盐酸等体积混合,在混合溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) | |
| C. | 等体积、等浓度的HR溶液和NaOH溶液混合,溶液中一定存在:c(Na+)>c(R-)>c(OH-)>c(H+) | |
| D. | 等体积、等浓度的①CH3COONa②NaNO3③NaClO溶液中离子总数:②>①>③ |
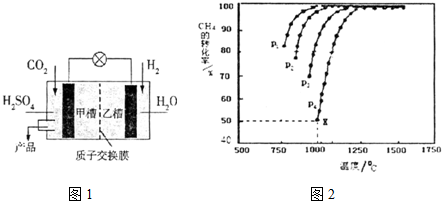 第21届联合国气候大会于2015年11月30日在巴黎召开,会议的主题是减 少温室气体排放量.
第21届联合国气候大会于2015年11月30日在巴黎召开,会议的主题是减 少温室气体排放量.