题目内容
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、含有 NA个氦原子的氦气(氦气是单原子分子)在标准状况下的体积约为11.2L |
| B、在标准状况下,11.2L H2O含有的分子数为0.5NA |
| C、在常温常压下,11.2L Cl2含有的分子数为0.5NA |
| D、.25℃,1.01×105Pa,64g SO2中含有的原子数为3NA |
考点:阿伏加德罗常数
专题:
分析:A.氦气为单原子分子;
B.气体摩尔体积适用对象为气体;
C.常温常用,Vm≠22.4L/mol;
D.质量转化成物质的量,结合二氧化硫分子的构成.
B.气体摩尔体积适用对象为气体;
C.常温常用,Vm≠22.4L/mol;
D.质量转化成物质的量,结合二氧化硫分子的构成.
解答:
解:A.氦气为单原子分子,含有 NA个氦原子的氦气,物质的量为1mol,标况下体积为22.4L,故A错误;
B.标准状况下,水为液体,不适用气体摩尔体积,故B错误;
C.常温常压下Vm≠22.4L/mol,11.2L Cl2的物质的量不是0.5mol,故C错误;
D.1个二氧化硫含有3个原子,64g SO2的物质的量=
=1mol,含有的原子数为3NA,故D正确;
故选:D.
B.标准状况下,水为液体,不适用气体摩尔体积,故B错误;
C.常温常压下Vm≠22.4L/mol,11.2L Cl2的物质的量不是0.5mol,故C错误;
D.1个二氧化硫含有3个原子,64g SO2的物质的量=
| 64g |
| 64g/mol |
故选:D.
点评:本题考查阿伏加德罗常数的有关计算和判断,明确标况下气体摩尔体积的使用条件,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系是解题关键,题目难度不大.

练习册系列答案
相关题目
去年年末,今年年初我国多省市遭遇雾霾笼罩,雾霾中含有大量的PM2.5,PM2.5首次被纳入标准.PM,英文全称为particulate matter(颗粒物),可吸入颗粒物又称为PM10,PM2.5又称为“细颗粒物”,下列说法不正确的是( )
| A、PM2.5值越大,形成雾霾天气的可能性越大 |
| B、PM2.5容易附着有毒有害物质,尤其是重金属,对人体造成危害 |
| C、城市由于汽车尾气的大量排放,比农村形成雾霾天气的可能性更大 |
| D、氟利昂作制冷剂会加剧雾霾天气的形成 |
往明矾[KAl(SO4)2?12H2O]溶液中滴入Ba(OH)2溶液,当只有一半的硫酸根离子恰好完全沉淀时,铝元素的存在形式为( )
| A、一部分为Al(OH)3,一部分为Al3+ |
| B、全部为Al(OH)3 |
| C、一部分为Al(OH)3,一部分为AlO2- |
| D、全部为AlO2- |
如图是常见四种有机物的比例模型示意图.下列说法正确的是( )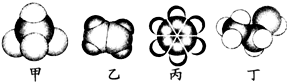

| A、甲能使酸性高锰酸钾溶液褪色 |
| B、乙可与溴水发生取代反应使溴水褪色 |
| C、丙中的碳碳键是介于碳碳单键和碳碳双键之间的独特的共价键 |
| D、丁与乙酸都能发生发生中和反应 |
工业利用冶铜炉渣(含Fe2O3、FeO、SiO2、Al2O3等)制Fe2O3的生产流程示意图:炉渣
滤液
沉淀
氧化铁,经“足量的NaOH溶液”处理后,铝元素的存在形态为( )
| 盐酸浸泡 |
| 过滤 |
| 氧化处理 |
| 足量的 |
| NaOH溶液 |
| 过滤 |
| 洗涤 |
| 煅烧 |
| A、Al |
| B、Al(OH)3 |
| C、Al3+ |
| D、[Al(OH)4]- |
下列叙述中正确的是( )
| A、含a mol AlCl3的溶液和含1.5a mol NaOH的溶液,无论正滴和反滴,生成的Al(OH)3的质量相等 |
| B、含a mol Na2CO3的溶液和含1.5a mol HCl的稀盐酸,无论正滴和反滴,生成的CO2相等 |
| C、等质量的NaHCO3和Na2CO3分别与足量盐酸反应,在同温同压下,生成的CO2体积相同 |
| D、二份质量相等组成不同的铝钠合金分别投入到足量盐酸中,若放出的H2越多,则铝的质量分数越小 |

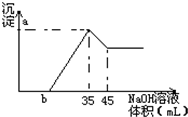 准确称取6g铝土矿(含Al2O3,Fe2O3,SiO2)样品,放入盛有100mLH2SO4溶液的烧杯中,充分反应后过滤,向滤液中加入10mol/LNaOH溶液,产生沉淀的量与所加NaOH溶液的体积关系如图所示.试求:
准确称取6g铝土矿(含Al2O3,Fe2O3,SiO2)样品,放入盛有100mLH2SO4溶液的烧杯中,充分反应后过滤,向滤液中加入10mol/LNaOH溶液,产生沉淀的量与所加NaOH溶液的体积关系如图所示.试求: