题目内容
9.实验需要0.1mol•L-1的 NaOH溶液500mL,其操作有以下各步:①用托盘天平称量NaOH的质量
②洗涤烧杯和玻璃棒2-3次,将洗涤液转入容量瓶中
③将冷却后的氢氧化钠溶液转移入容量瓶中
④将NaOH倒入烧杯中用水溶解、冷却
⑤加水至液面接近刻度线1~2cm处,定容,摇匀
完成下列填空:
(1)实验中除了托盘天平、烧杯、玻璃棒外还需要的其他仪器有玻璃棒、胶头滴管.
(2)根据计算得知,所需NaOH的质量为2.0g.
(3)正确的操作顺序是①④③②⑤(用序号填写)
(4)配制过程中,下列情况会使配制结果偏低的是③④.
①定容时俯视刻度线观察液面
②未经冷却就进行转移操作
③移液时未洗涤烧杯和玻璃棒
④定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线.
(5)若取50.0mL上述已配好的溶液,与另一150mL0.2mol/L的NaOH溶液混合,最后得到的溶液的物质的量浓度为0.175mol/L(设溶液的体积变化可忽略).
分析 (1)依据配制一定物质的量浓度溶液一般步骤选择需要仪器;
(2)依据m=CVM计算需要溶质的质量;
(3)配制一定物质的量浓度溶液一般步骤:计算、称量(量取)、溶解(稀释)、冷却、移液、洗涤、定容、摇匀,据此排序;
(4)分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析;
(5)根据溶液稀释前后溶质的量不变;
解答 解:(1)配制一定物质的量浓度溶液一般步骤:计算、称量(量取)、溶解(稀释)、移液、洗涤、定容、摇匀等,用到的仪器:托盘天平(量筒)、药匙、烧杯、玻璃棒、容量瓶、胶头滴管,还需要的仪器:玻璃棒、胶头滴管;
故答案为:玻璃棒、胶头滴管;
(2)需要0.1mol•L-1的 NaOH溶液500mL,需要溶质的质量m=0.1mol/L×0.5L×40g/mol=2.0g;
故答案为:2.0g;
(3)配制一定物质的量浓度溶液一般步骤:计算、称量(量取)、溶解(稀释)、冷却、移液、洗涤、定容、摇匀,所以正确的顺序为:①④③②⑤;
(4)①定容时俯视刻度线观察液面,导致溶液体积偏小,溶液浓度偏高,故不选;
②未经冷却就进行转移操作,冷却后,液面下降,溶液体积偏小,溶液浓度偏高,故不选;
③移液时未洗涤烧杯和玻璃棒,导致溶质的物质的量偏小,溶液浓度偏低,故选;
④定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线,导致溶液体积偏大,溶液浓度偏低,故选;
故选:③④;
(5)若取50.0mL上述已配好的溶液,与另一150mL0.200mol/L的Na2CO3溶液混合,最后得到的溶液的物质的量浓度为$\frac{0.1×50+0.2×150}{200}$=0.175 mol/L,
故答案为:0.175 mol/L.
点评 本题考查了一定物质的量浓度溶液配制,明确配制原理及操作步骤是解题关键,注意容量瓶构造及使用方法、注意事项,题目难度不大.

| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅥⅠA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)画出原子的结构示意图:④
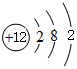 ,⑤
,⑤ .
.(3)在这些元素中,最活泼的金属元素是K,最活泼的非金属元素是F,最不活泼的元素是Ar.(均用元素符号表示)
(4)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.(均写出物质的化学式)
| A. | 分液时,分液漏斗的上层液体应由上口到出 | |
| B. | 向某溶液中加入稀盐酸,产生的气体通入澄清石灰水,石灰水变浑浊,该溶液一定是碳酸盐溶液 | |
| C. | 配置0.1000mol•L-1氢氧化钠溶液时,将液体转移到容量瓶中需用玻璃棒引流 | |
| D. | 锥形瓶用作反应容器时可以加热 |
| 温度/℃ | 1 000 | 1 150 | 1 300 |
| 平衡常数 | 64.0 | 50.7 | 42.9 |
该反应的平衡常数表达式K=$\frac{{c}^{3}(C{O}_{2})}{{c}^{3}(CO)}$,△H<0(填“>”、“<”或“=”).
Ⅱ、工业上利用CO和水蒸气在一定条件下发生反应制取氢气:
CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41kJ/mol
某小组研究在相同温度下该反应过程中的能量变化.他们分别在体积均为V L的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应.相关数据如表:
| 容器编号 | 起始时各物质物质的量/mol | 达到平衡的时间/min | 达平衡时体系能量的变化/kJ | ||||
| CO | H2O | CO2 | H2 | ||||
| ① | 1 | 4 | 0 | 0 | t1 | 放出热量:32.8 kJ | |
| ② | 2 | 8 | 0 | 0 | t2 | 放出热量:Q | |
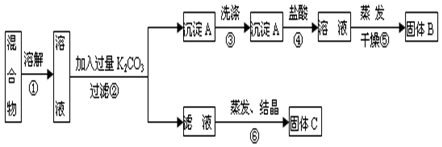
(2)计算容器②中反应的平衡常数K=1.
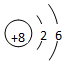 、
、