题目内容
物质A是工业生产水泥、玻璃的重要物质之一、也是煤脱硫中所使用的物质.物质A能与醋酸反应生成物质B,B属于温室气体,将B气体通入澄清的石灰水时,澄清的石灰水先变浑浊后澄清得物质C.若将该澄清溶液加热又变浑浊生成物质A.请写出下列反应的离子方程式
(1)A与醋酸反应的离子方程式
(2)气体B使澄清的石灰水变浑浊的离子方程式
(3)向上述所得浑浊的液体中继续通入气体B使液体又变澄清的离子方程式
(4)将气体B通入硅酸钠溶液中生成白色沉淀(硅 酸H2SiO3)的离子方程式 .
(1)A与醋酸反应的离子方程式
(2)气体B使澄清的石灰水变浑浊的离子方程式
(3)向上述所得浑浊的液体中继续通入气体B使液体又变澄清的离子方程式
(4)将气体B通入硅酸钠溶液中生成白色沉淀(硅 酸H2SiO3)的离子方程式
考点:离子方程式的书写
专题:离子反应专题
分析:工业生产水泥、玻璃、煤脱硫中都用到的物质是碳酸钙,碳酸钙与醋酸反应生成二氧化碳,二氧化碳通入到澄清石灰水,首先反应生成碳酸钙,继续通入二氧化碳,碳酸钙与二氧化碳和水反应生成碳酸氢钙,碳酸的酸性强于硅酸,所以将二氧化碳硅酸钠溶液中生成硅酸和碳酸钠,据此解答.
解答:
解:(1)碳酸钙与醋酸反应的离子方程式为:CaCO3+2CH3COOH=2CH3COO-+Ca2++CO2↑+H2O;
故答案为:CaCO3+2CH3COOH=2CH3COO-+Ca2++CO2↑+H2O;
(2)二氧化碳使澄清的石灰水变浑浊的离子方程式:Ca2++2OH-+CO2=CaCO3↓+H2O;
故答案为:Ca2++2OH-+CO2=CaCO3↓+H2O;
(3)碳酸钙与水、二氧化碳反应的离子方程式为:CaCO3↓+H2O+CO2=Ca2++2HCO3-;
故答案为:CaCO3↓+H2O+CO2=Ca2++2HCO3-;
(4)二氧化碳通入硅酸钠溶液中反应的离子方程式为:CO2+SiO32-+H2O=H2SiO3↓+CO32-;
故答案为:CO2+SiO32-+H2O=H2SiO3↓+CO32-.
故答案为:CaCO3+2CH3COOH=2CH3COO-+Ca2++CO2↑+H2O;
(2)二氧化碳使澄清的石灰水变浑浊的离子方程式:Ca2++2OH-+CO2=CaCO3↓+H2O;
故答案为:Ca2++2OH-+CO2=CaCO3↓+H2O;
(3)碳酸钙与水、二氧化碳反应的离子方程式为:CaCO3↓+H2O+CO2=Ca2++2HCO3-;
故答案为:CaCO3↓+H2O+CO2=Ca2++2HCO3-;
(4)二氧化碳通入硅酸钠溶液中反应的离子方程式为:CO2+SiO32-+H2O=H2SiO3↓+CO32-;
故答案为:CO2+SiO32-+H2O=H2SiO3↓+CO32-.
点评:本题考查了离子方程式的书写,熟悉二氧化碳的性质是解题关键,注意硅酸为沉淀.

练习册系列答案
相关题目
把Ba(OH)2溶液逐滴滴入明矾[KAl(SO4)2?12H2O]溶液中,可能发生的离子方程式是( )
| A、2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ |
| B、A13++2SO42-+2Ba2++3OH-=A1(0H)3↓+2BaSO4↓ |
| C、2Ba2++4OH-+Al3++2SO42-=2BaSO4↓+AlO2-+2H2O |
| D、Ba2++3OH-+Al3++SO42-=BaSO4↓+A1(0H)3↓ |
将含有0.20mol的碳酸钠的液体逐滴加入到200mL的某浓度的盐酸溶液中,有标准状况下3.36L的气体产生,若改将该盐酸溶液逐滴加入原碳酸钠溶液中,则产生标况下气体的体积为( )
| A、0L | B、2.24L |
| C、3.36L | D、4.48L |
在0.6mol Ba(OH)2中,含有OH-的数目是( )
| A、约为1.2 |
| B、约为7.22×1023 |
| C、约为6.02×1023 |
| D、约为3.01×1023 |
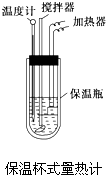 在量热计中将100mL 0.50mol?L-1的CH3COOH溶液与100mL 0.55mol?L-1的NaOH溶液混合,温度从298.0K升高至300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要的热量)是150.5J?K-1,溶液密度均为1g?mL-1,生成溶液的比热容c=4.184J?(g?K)-1.
在量热计中将100mL 0.50mol?L-1的CH3COOH溶液与100mL 0.55mol?L-1的NaOH溶液混合,温度从298.0K升高至300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要的热量)是150.5J?K-1,溶液密度均为1g?mL-1,生成溶液的比热容c=4.184J?(g?K)-1.