题目内容
某同学按下列步骤配制500 mL 0.20 mol/LKCl溶液,请回答有关问题.
(1)计算所需KCl的质量 需要KCl的质量为 g
(2)称量KCl固体,称量过程中主要用到的仪器是
(3)将KCl加入100 mL烧杯中,加适量蒸馏水溶解 为加快溶解,可采取的措施是
(4)将烧杯中的溶液转移至500 mL容量瓶中 为防止溶液溅出,应该采取的措施是
(5)向容量瓶中加蒸馏水至刻度线 在进行此操作时应注意的问题
(6)你认为按上述步骤配制的KCl溶液的浓度是否为0.20 mol/L,请说明理由 .
(1)计算所需KCl的质量 需要KCl的质量为
(2)称量KCl固体,称量过程中主要用到的仪器是
(3)将KCl加入100 mL烧杯中,加适量蒸馏水溶解 为加快溶解,可采取的措施是
(4)将烧杯中的溶液转移至500 mL容量瓶中 为防止溶液溅出,应该采取的措施是
(5)向容量瓶中加蒸馏水至刻度线 在进行此操作时应注意的问题
(6)你认为按上述步骤配制的KCl溶液的浓度是否为0.20 mol/L,请说明理由
考点:配制一定物质的量浓度的溶液
专题:实验题
分析:(1)利用n=cV计算出氯化钾的物质的量,再根据m=nM计算所需氯化钾的质量;
(2)一般用托盘天平称量固体质量,用药匙取用药品;
(3)加热、搅拌、将氯化钾研细等可以加速溶解;
(4)为防止溶液溅出通常采取用玻璃棒引流;
(5)定容应注意:加水至液面距离刻度线1~2cm时,改用胶头滴管滴加至溶液凹液面与刻度线水平相切;
(6)配制操作过程缺少洗涤烧杯、玻璃棒,少量氯化钾粘在烧杯、玻璃棒上.
(2)一般用托盘天平称量固体质量,用药匙取用药品;
(3)加热、搅拌、将氯化钾研细等可以加速溶解;
(4)为防止溶液溅出通常采取用玻璃棒引流;
(5)定容应注意:加水至液面距离刻度线1~2cm时,改用胶头滴管滴加至溶液凹液面与刻度线水平相切;
(6)配制操作过程缺少洗涤烧杯、玻璃棒,少量氯化钾粘在烧杯、玻璃棒上.
解答:
解:(1)需氯化钾的质量为m=0.5L×0.2mol?L-1×74.5g/mol=7.45g≈7.5g,故答案为:7.5;
(2)通常用托盘天平称量,用药匙取氯化钾,故答案为:托盘天平、药匙;
(3)为加快氯化钾溶解可以采取搅拌、加热、研细氯化钾等措施.
故答案为:搅拌、加热、研细氯化钾等措施;
(4)为防止溶液溅出通常采取用玻璃棒引流,故答案为:玻璃棒引流;
(5)定容应注意:加水至液面距离刻度线1~2cm时,改用胶头滴管滴加至溶液凹液面与刻度线水平相切,
故答案为:加水至液面距离刻度线1~2cm时,改用胶头滴管滴加至溶液凹液面与刻度线水平相切;
(6)配制操作过程缺少洗涤烧杯、玻璃棒,少量氯化钾粘在烧杯、玻璃棒上,移入容量瓶中氯化钾的质量减小,所配溶液浓度偏低,
故答案为:低于0.2 mol?L-1,未洗涤烧杯和玻璃棒.
(2)通常用托盘天平称量,用药匙取氯化钾,故答案为:托盘天平、药匙;
(3)为加快氯化钾溶解可以采取搅拌、加热、研细氯化钾等措施.
故答案为:搅拌、加热、研细氯化钾等措施;
(4)为防止溶液溅出通常采取用玻璃棒引流,故答案为:玻璃棒引流;
(5)定容应注意:加水至液面距离刻度线1~2cm时,改用胶头滴管滴加至溶液凹液面与刻度线水平相切,
故答案为:加水至液面距离刻度线1~2cm时,改用胶头滴管滴加至溶液凹液面与刻度线水平相切;
(6)配制操作过程缺少洗涤烧杯、玻璃棒,少量氯化钾粘在烧杯、玻璃棒上,移入容量瓶中氯化钾的质量减小,所配溶液浓度偏低,
故答案为:低于0.2 mol?L-1,未洗涤烧杯和玻璃棒.
点评:本题考查了一定物质的量浓度溶液的配制、根据方程式计算,难度不大,注意从c=
理解配制原理,注意托盘天平精确度为0.1.
| n |
| V |

练习册系列答案
相关题目
下面有关Na2CO3 与NaHCO3的性质比较中错误的是( )
| A、相同质量时消耗的HCl:Na2CO3>NaHCO3 |
| B、相同物质的量时消耗的HCl:Na2CO3>NaHCO3 |
| C、与同浓度的硫酸反应放出气泡的速率:NaHCO3<Na2CO3 |
| D、热稳定性:NaHCO3<Na2CO3 |
已知某合金(仅含铜、铁)中铜和铁的物质的量之和为y mol,其中Cu的物质的量分数为a,将其全部投入50mL b mol?L-1的硝酸溶液中,加热使其充分反应(假设NO是唯一的还原产物).下列说法正确的是( )
| A、若金属没有剩余,反应中转移的电子数目为2y NA | ||
| B、若金属全部溶解,则溶液中一定含有Fe3+ | ||
C、当溶液中金属离子只有Fe3+、Cu2+时,则a与b的关系为:b≥80y(1-
| ||
| D、若金属全部溶解,且产生336mL气体(标准状况),则b=0.3 |

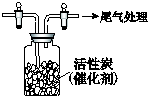 某学习小组依据SO2具有还原性,推测SO2能被Cl2氧化生成SO2Cl2.
某学习小组依据SO2具有还原性,推测SO2能被Cl2氧化生成SO2Cl2.