题目内容
关于下列图示的说法中正确的( )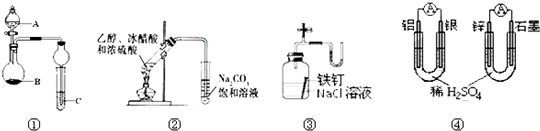

| A、图①中,若A为浓盐酸,B为MnO2,C中盛石蕊试液,则C中溶液先变红后褪色 |
| B、图②制备乙酸乙酯 |
| C、图③证明铁生锈与空气有关 |
| D、图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量也相同 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.在加热条件下,浓盐酸和二氧化锰反应生成氯气,不加热时二者不反应;
B.制取乙酸乙酯时,导气管不能伸入碳酸钠溶液中;
C.根据U形管中液体变化确定是否与空气有关;
D.每个铝原子和锌原子失去电子数不等.
B.制取乙酸乙酯时,导气管不能伸入碳酸钠溶液中;
C.根据U形管中液体变化确定是否与空气有关;
D.每个铝原子和锌原子失去电子数不等.
解答:
解:A.在加热条件下,浓盐酸和二氧化锰反应生成氯气,不加热时二者不能生成氯气,所以只有挥发出的氯化氢,氯化氢使紫色石蕊试液变红色,故A错误;
B.制取乙酸乙酯时,导气管不能伸入碳酸钠溶液中,否则易产生倒吸现象,且不利于收集乙酸乙酯,故B错误;
C.如果铁钉发生吸氧腐蚀,则U形管中左端液柱上升,从而确定铁钉的腐蚀与空气有关,故C正确;
D.每个铝原子和锌原子失去电子数不等,所以两个装置是通过导线的电子数相等时,消耗的负极材料的物质的量不等,故D错误;
故选C.
B.制取乙酸乙酯时,导气管不能伸入碳酸钠溶液中,否则易产生倒吸现象,且不利于收集乙酸乙酯,故B错误;
C.如果铁钉发生吸氧腐蚀,则U形管中左端液柱上升,从而确定铁钉的腐蚀与空气有关,故C正确;
D.每个铝原子和锌原子失去电子数不等,所以两个装置是通过导线的电子数相等时,消耗的负极材料的物质的量不等,故D错误;
故选C.
点评:本题考查了化学实验评价,涉及氯气的制取、乙酸乙酯的制取、铁钉的吸氧腐蚀、原电池原理等知识点,明确实验原理是解本题关键,根据物质的性质分析解答,易错选项是A,注意只有加热时二者才能生成氯气,否则不能生成氯气,且稀盐酸和二氧化锰在加热条件下也不能产生氯气,为易错点.

练习册系列答案
相关题目
用NA表示阿伏加德罗常数,下列说法正确的是( )
| A、18g D2O含有电子数为9NA |
| B、标准状况下,11.2L乙酸中含有的分子数目为0.5NA |
| C、78g Na2O2中含有的离子总数为4NA |
| D、1L 1mol?L-1 Na2CO3溶液中,溶液中CO32-离子数是NA |
将x mol O2、y mol CH4、z mol Na2O2投入密闭容器内,在150℃条件下,电火花引发反应后,反应物均无剩余,容器内压强为零,则下列x、y、z之间的关系式中正确的是( )
| A、Z=3X+2Y |
| B、4Y=2X+Z |
| C、3X=Y+5Z |
| D、6Y=2X+Z |
NA代表阿伏加德罗常数,下列说法正确的是( )
| A、2mol Na被完全氧化生成1mol Na2O2,得到2NA个电子 |
| B、25℃时pH=13的NaOH液中含有OH一的数目为0.1NA |
| C、标准状况下,6.72L NO2与水充分反应转移的电子数目为0.1NA |
| D、等物质的量的HCN与NaCN混合后溶液显碱件.则溶液中c(CN-)<c(HCN) |

 电渗析法淡化海水示意图如图所示,其中阴(阳)离子交换膜仅允许阴(阳)离子通过.
电渗析法淡化海水示意图如图所示,其中阴(阳)离子交换膜仅允许阴(阳)离子通过.
 A、B、C是中学化学中常见的三种元素(A、B、C代表元素符号).A位于元素周期表中第4周期,其基态原子最外层电子数为2且内层轨道全部排满电子.短周期元素B的一种常见单质为淡黄色粉末.元素C的原子最外层电子数是其内层电子数的3倍.
A、B、C是中学化学中常见的三种元素(A、B、C代表元素符号).A位于元素周期表中第4周期,其基态原子最外层电子数为2且内层轨道全部排满电子.短周期元素B的一种常见单质为淡黄色粉末.元素C的原子最外层电子数是其内层电子数的3倍.