题目内容
用NA表示阿伏加德罗常数,下列说法正确的是( )
| A、18g D2O含有电子数为9NA |
| B、标准状况下,11.2L乙酸中含有的分子数目为0.5NA |
| C、78g Na2O2中含有的离子总数为4NA |
| D、1L 1mol?L-1 Na2CO3溶液中,溶液中CO32-离子数是NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.重水的摩尔质量为20g/mol,重水中含有10个电子;
B.标准状况下乙酸不是气体,不能使用标况下的气体摩尔体积计算其物质的量;
C.过氧化钠中阴离子为过氧根离子,1mol过氧化钠中含有1mol阴离子;
D.碳酸钠溶液中,碳酸根离子部分水解,碳酸根离子数目减少.
B.标准状况下乙酸不是气体,不能使用标况下的气体摩尔体积计算其物质的量;
C.过氧化钠中阴离子为过氧根离子,1mol过氧化钠中含有1mol阴离子;
D.碳酸钠溶液中,碳酸根离子部分水解,碳酸根离子数目减少.
解答:
解:A.18g重水的物质的量为0.9mol,0.9mol重水中含有9mol电子,含有电子数为9NA,故A正确;
B.标况下,乙酸不是气体,题中条件无法计算11.2L乙酸的物质的量,故B错误;
C.78g过氧化钠的物质的量为1mol,1mol过氧化钠中含有2mol钠离子、1mol过氧根离子,总共含有3mol离子,含有的离子总数为3NA,故C错误;
D.1L 1mol?L-1 Na2CO3溶液中含有溶质碳酸钠1mol,由于碳酸根离子部分水解,溶液中碳酸根离子的物质的量小于1mol,溶液中CO32-离子数小于NA,故D错误;
故选A.
B.标况下,乙酸不是气体,题中条件无法计算11.2L乙酸的物质的量,故B错误;
C.78g过氧化钠的物质的量为1mol,1mol过氧化钠中含有2mol钠离子、1mol过氧根离子,总共含有3mol离子,含有的离子总数为3NA,故C错误;
D.1L 1mol?L-1 Na2CO3溶液中含有溶质碳酸钠1mol,由于碳酸根离子部分水解,溶液中碳酸根离子的物质的量小于1mol,溶液中CO32-离子数小于NA,故D错误;
故选A.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下乙酸、水、三氧化硫等不是气体,过氧化钠中的阴离子为过氧根离子.

练习册系列答案
相关题目
部分弱酸的电离平衡常数如下表,下列选项错误的是( )
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 (25℃) |
Ka=1.8×10-5 | Ka=4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
| A、CN-+H2O+CO2=HCN+HCO3- |
| B、2CH3COOH+CO32-=2CH3COO-+H2O+CO2↑ |
| C、中和等体积、等pH的CH3COOH和HCN消耗NaOH的量前者小于后者 |
| D、等体积、等浓度的CH3COONa和NaCN溶液中所含离子总数前者小于后者 |
实验是研究化学的基础,下图中所示的实验方法、装置或操作完全正确的是( )
A、 检查气密性 |
B、 吸收HCl |
C、 制取Fe(OH)2沉淀 |
D、 稀释浓H2SO4 |
在体积相同的两个密闭容器中分别充满NO、NO2,当这两个容器内温度和气体密度相等时,下列说法正确的是( )
| A、两种气体的压强相等 |
| B、两种气体的氮原子数目不相等 |
| C、两种气体的分子数目相等 |
| D、NO比NO2的质量小 |
用图甲装置电解一定量的CuSO4溶液,M、N为惰性电极.电解过程实验数据如图乙所示.X轴表示电解过程中转移电子的物质的量,Y轴表示电解过程产生气体的总体积.则下列说法不正确的是( )


| A、电解过程中N电极表面先有红色物质生成,后有气泡产生 |
| B、A点所得溶液只需加入一定量的CuO固体就可恢复到起始状态 |
| C、Q点时M、N两电极上产生的气体在相同条件下体积相同 |
| D、若M电极材料换成Cu做电极,则电解过程中CuSO4溶液的浓度不变 |
下列离子方程式书写不正确的是( )
| A、等物质的量的 CO2与氢氧化钠溶液反应:CO2+OH-=HCO3- | ||||
| B、少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO | ||||
| C、Ca(OH)2溶液与等物质的量的稀H2SO4混合:Ca2++2OH-+2H++SO42-═CaSO4↓+2H2O | ||||
D、用石墨电极电解饱和食盐水:2H2O+2Cl-
|
关于下列图示的说法中正确的( )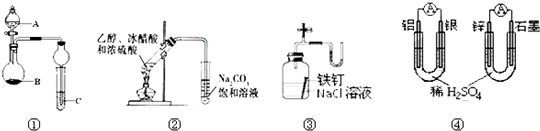

| A、图①中,若A为浓盐酸,B为MnO2,C中盛石蕊试液,则C中溶液先变红后褪色 |
| B、图②制备乙酸乙酯 |
| C、图③证明铁生锈与空气有关 |
| D、图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量也相同 |
