题目内容
1.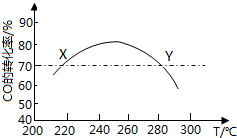 工业上,利用CO和H2合成二甲醚:3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)在合适的温度下,研究者进行了多次实验,每次实验保持原料气组成(3molCO、3molH2)、体积(10L)、反应时间等因素不变,实验结果如图所示.下列说法正确的是( )
工业上,利用CO和H2合成二甲醚:3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)在合适的温度下,研究者进行了多次实验,每次实验保持原料气组成(3molCO、3molH2)、体积(10L)、反应时间等因素不变,实验结果如图所示.下列说法正确的是( )| A. | X、Y两点对应的CO正反应速率相等 | |
| B. | 合成二甲醚的正反应△H>0 | |
| C. | 反应温度应控制在240℃~260℃之间 | |
| D. | 选择合适催化剂,可以提高CO转化率 |
分析 A.温度不同,反应速率不同;
B.转化率达到最高点之后,升高温度转化率降低,说明升高温度平衡逆向移动;
C.240℃~260℃之间转化率最高;
D.催化剂不影响平衡移动.
解答 解:A.X、Y两点对应的温度不同,反应速率不同,故A错误;
B.转化率达到最高点之后,升高温度转化率降低,说明升高温度平衡逆向移动,可说明反应为放热反应,故B错误;
C.240℃~260℃之间转化率最高,故C正确;
D.催化剂不影响平衡移动,转化率不变,故D错误.
故选C.
点评 本题考查化学反应平衡移动以及反应速率等知识,为高频考点,侧重于学生的分析能力的考查,注意把握图象的变化趋势以及影响因素等知识,难度不大.

练习册系列答案
相关题目
11.如图为某高效锂硫电池.关于该电池的说法正确的是( )


| A. | 电子流向:B电极→用电器→A电极→电解质→B电极 | |
| B. | A电极上发生的一个电极反应为:2Li++S8+2e-═Li2S8 | |
| C. | 若用该电池在铁器上镀锌,电路中转移2 moI电子时,电镀池两电极质量差为65 g | |
| D. | 若用该电池电解精炼铜,负极减少7g时阳极减少质量为32 g |
12.某有机物的结构简式如图所示,有关该有机物的叙述不正确的是( )


| A. | 在一定条件下,能发生取代、氧化和加聚反应 | |
| B. | 该物质分子中最多可以有11个碳原子在同一平面上 | |
| C. | 1 mol该物质最多可与5 mol H2发生加成反应 | |
| D. | 1 mol该物质完全氧化最多可消耗13 mol氧气 |
6. 如图,在盛有稀硫酸的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )
如图,在盛有稀硫酸的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )
 如图,在盛有稀硫酸的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )
如图,在盛有稀硫酸的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )| A. | 外电路的电流方向为X→外电路→Y | |
| B. | 若两电极都是金属,则它们的活动性顺序为X<Y | |
| C. | X极上发生的是还原反应,Y极上发生的是氧化反应 | |
| D. | SO42-向X电极移动 |
13.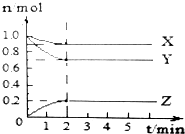 某温度时,在1L恒容密闭容器中X、Y、Z三种气体的物质的量随时间变化曲线如图所示,以下说法正确的是( )
某温度时,在1L恒容密闭容器中X、Y、Z三种气体的物质的量随时间变化曲线如图所示,以下说法正确的是( )
 某温度时,在1L恒容密闭容器中X、Y、Z三种气体的物质的量随时间变化曲线如图所示,以下说法正确的是( )
某温度时,在1L恒容密闭容器中X、Y、Z三种气体的物质的量随时间变化曲线如图所示,以下说法正确的是( )| A. | 反应开始至2min,反应的平均速率v(Z)=0.2mol/L | |
| B. | 该反应的化学方程式为X+3Y═2Z | |
| C. | 该反应平衡时,Y转化率为30% | |
| D. | 3min时,充入X,v正增大,v逆减小 |
15.航天科学技术测得,三氧化二碳(C2O3)是金星大气层的成分之一.下列说法正确的是( )
| A. | C2O3和CO2是同素异形体 | B. | C2O3和CO完全燃烧,产物都是CO2 | ||
| C. | C2O3和CO都是酸性氧化物 | D. | C2O3和CO2互为同分异构体 |