题目内容
11.如图为某高效锂硫电池.关于该电池的说法正确的是( )
| A. | 电子流向:B电极→用电器→A电极→电解质→B电极 | |
| B. | A电极上发生的一个电极反应为:2Li++S8+2e-═Li2S8 | |
| C. | 若用该电池在铁器上镀锌,电路中转移2 moI电子时,电镀池两电极质量差为65 g | |
| D. | 若用该电池电解精炼铜,负极减少7g时阳极减少质量为32 g |
分析 在原电池中,电解质里的阳离子移向正极,所以A是正极,发生还原反应:2Li++S8+2e-═Li2S8,电子从原电池的负极流向正极,根据电镀吃、电解精炼铜装置的特点以及电极反应式结合电子转移进行计算即可.
解答 解:A、在原电池中,电解质里的阳离子移向正极,所以A是正极,发生还原反应,B是负极,发生氧化反应,电子从负极流向正极,电子从B电极经过外电路流向A电极,但是电子不会经过电解质溶液,故A错误;
B、A是正极,发生得电子的还原反应:2Li++S8+2e-═Li2S8,故B正确;
C、电镀池的特点:阳极质量减小量等于阴极质量增加量,故C错误;
D、若用该电池电解精炼铜,负极减少7g时,即转移电子是1mol,阳极减少质量不是金属铜,而是比金属铜活泼的金属,所以质量减小量不是32g,故D错误.
故选B.
点评 本题考查化学电源新型电池,题目难度中等,注意把握原电池的工作原理和电极反应的判断.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
1.化学与科学、技术、社会、环境、生活密切相关.下列有关说法中错误的是( )
| A. | CCTV-8法兰琳卡护肤产品广告中“我们恨化学”严重违反科学,因其工艺肯定与化学有关 | |
| B. | 智能手机中使用的石墨烯不仅是电和热的良导体,还是硬度较大的新型有机合成材料 | |
| C. | 采用催化转换技术将汽车尾气中的NOx和CO转化为无毒气体 | |
| D. | 为了能增加水中氧气的含量,养金鱼用的自来水一般先在阳光下晒一段时间 |
2.向四支试管中分别加入少量不同的无色溶液进行如下操作,现象和结论正确的是( )
| 操作 | 现象 | 结论 | |
| A. | 先滴加BaCl2溶液再滴加HCl溶液 | 生成白色沉淀 | 原溶液中有SO42- |
| B. | 先滴加稀盐酸再滴加AgNO3溶液 | 生成白色沉淀 | 原溶液中有Cl- |
| C. | 用洁净铁丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有Na+ |
| D. | 滴加NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
| A. | A | B. | B | C. | C | D. | D |
19.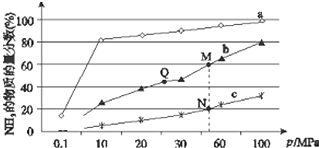 已知合成氨反应N2(g)+3H2?NH3(g)△H<0,当反应器中按n(N2):n(H2)=1:3投料后,在不同温度下,反应达到平衡时,得到混合物中NH3的物质的量分数随压强的变化曲线a、b、c如图所示.下列说法正确的是( )
已知合成氨反应N2(g)+3H2?NH3(g)△H<0,当反应器中按n(N2):n(H2)=1:3投料后,在不同温度下,反应达到平衡时,得到混合物中NH3的物质的量分数随压强的变化曲线a、b、c如图所示.下列说法正确的是( )
 已知合成氨反应N2(g)+3H2?NH3(g)△H<0,当反应器中按n(N2):n(H2)=1:3投料后,在不同温度下,反应达到平衡时,得到混合物中NH3的物质的量分数随压强的变化曲线a、b、c如图所示.下列说法正确的是( )
已知合成氨反应N2(g)+3H2?NH3(g)△H<0,当反应器中按n(N2):n(H2)=1:3投料后,在不同温度下,反应达到平衡时,得到混合物中NH3的物质的量分数随压强的变化曲线a、b、c如图所示.下列说法正确的是( )| A. | 曲线a对应的反应温度最高 | |
| B. | 上图中M、N、Q点平衡常数K的大小关系为K(M)=K(Q)<K(N) | |
| C. | 相同压强下,投料相同,达到平衡所需时间关系为c>b>a | |
| D. | N点时c(NH3)=0.2 mol/L,则N点的c(N2):c(NH3)=1:1 |
16.下列说法正确的是( )
| A. | 反应2Mg+CO2$\frac{\underline{\;\;△\;\;}}{\;}$2MgO+C△H<0从熵变角度看,可自发进行 | |
| B. | 在密闭容器发生可逆反应:2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-113.0 kJ/mol,达到平衡后,保持温度不变,缩小容器体积,重新达到平衡后,△H变小 | |
| C. | 已知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=2.0×10-12,将等体积浓度为1.0×10-4mol/L的AgNO3溶液滴入到浓度均为1.0×10-4mol/L的KCl和K2CrO4的混合溶液中产生两种不同沉淀,且Ag2CrO4沉淀先产生 | |
| D. | 根据HClO的Ka=3.0×10-8,H2CO3的Ka1=4.3×10-7,Ka2=5.6×10-11,可推测相同状况下,等浓度的NaClO与Na2CO3溶液中,pH前者小于后者 |
3.用NA表示阿伏伽德罗常数的值,下列叙述中正确的是( )
| A. | 常温常压下,11.2L一氧化碳和二氧化碳混合气体中含有的碳原子数目为0.5NA | |
| B. | 标准状况下,7.1克氯气与足量的氢氧化钠溶液反应转移的电子数位0.2NA | |
| C. | 92克二氧化氮和四氧化二氮的混合气体中含有的原子总数为6NA | |
| D. | 1.5mol/L氯化钙溶液中含有氯离子数目为3NA |
20.下列相关反应的离子方程式书写正确的是( )
| A. | H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H+十SO42-═BaSO4↓+H2O | |
| B. | 将稀硝酸滴加到氯化银固体上:AgCl+H+═Ag++HCl | |
| C. | 向碳酸氢铵溶液中加过量石灰水并加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3•H2O | |
| D. | 用酸化的高锰酸钾溶液氧化双氧水:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O |
1.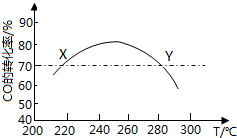 工业上,利用CO和H2合成二甲醚:3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)在合适的温度下,研究者进行了多次实验,每次实验保持原料气组成(3molCO、3molH2)、体积(10L)、反应时间等因素不变,实验结果如图所示.下列说法正确的是( )
工业上,利用CO和H2合成二甲醚:3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)在合适的温度下,研究者进行了多次实验,每次实验保持原料气组成(3molCO、3molH2)、体积(10L)、反应时间等因素不变,实验结果如图所示.下列说法正确的是( )
 工业上,利用CO和H2合成二甲醚:3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)在合适的温度下,研究者进行了多次实验,每次实验保持原料气组成(3molCO、3molH2)、体积(10L)、反应时间等因素不变,实验结果如图所示.下列说法正确的是( )
工业上,利用CO和H2合成二甲醚:3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)在合适的温度下,研究者进行了多次实验,每次实验保持原料气组成(3molCO、3molH2)、体积(10L)、反应时间等因素不变,实验结果如图所示.下列说法正确的是( )| A. | X、Y两点对应的CO正反应速率相等 | |
| B. | 合成二甲醚的正反应△H>0 | |
| C. | 反应温度应控制在240℃~260℃之间 | |
| D. | 选择合适催化剂,可以提高CO转化率 |