��Ŀ����
14��A��B��C�������ڱ��ж�����Ԫ����ɵ����ֳ���������ס��ҡ��������ֵ��ʣ���Щ���ʺͻ�����֮�������ͼ1��ʾ�Ĺ�ϵ��������пհף�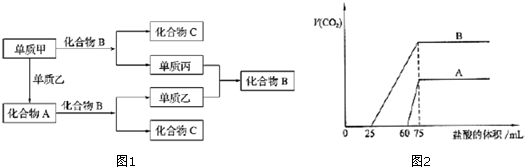
��1�����̪��Һ�м��뻯����A�ķ�ĩ������Ϊ��Һ�ȱ�����ɫ�������������ɣ�
��2�����ʼ��뻯����B��Ӧ�����ӷ���ʽΪ2Na+2H2O�T2Na++2OH-+H2��5.05g���ʼ�-�غϽ�����200mLˮ����0.075mol������ȷ���úϽ�Ļ�ѧʽNaK2��
��3����50mLijŨ�ȵĻ�����C����Һ��ͨ��CO2��������ҺM����CO2ͨ�����IJ�ͬ����ҺM�����Ҳ��ͬ������M����μ���0.1mol/L���ᣬ������������ ��F��CO2���������������F��HCl���Ĺ�ϵ����ͼ2ʾ���������
����Aȷ���μ�ǰ60mL������ʱ��������Ӧ�����ӷ���ʽOH-+H+=H2O��H++CO32-=HCO3-�����м���д��������
����Aͼ������ԭ��Һͨ��CO2�����������Һ�е����ʵĻ�ѧʽΪNa2CO3��NaOH��
��ԭ������C��Һ�����ʵ���Ũ��Ϊ0.15mol/L��
����A��B��֪������ʵ��ͨ���CO2�������Ϊ3��10��
���� A��B��C�������ڱ��ж�����Ԫ����ɵ����ֳ���������ס��ҡ��������ֵ��ʣ�����B��Ӧ���û���Ӧ���������ǻ��Ϸ�Ӧ��������Ҳ�ǻ��Ϸ�Ӧ�����ʼס����м�Ԫ�صĻ�����A���뻯����B��Ӧ�õ���ͬ�ĵ��ʣ������ֵ��ʷ�Ӧ�ֵõ�������B��Ӧ��Na������������ˮ�ķ�Ӧ������֪����Na���ʣ���Ϊ������B��H2O����Ϊ������C��NaOH��A��Na2O2���ݴ˽��
��1���������ƺ�ˮ��Ӧ�������������Ǽ�ʹ��̪��Һ���ɫ���������ƾ���Ư���Կ���ʹ��ɫ��ȥ��
��2�����ݵ���ת���غ��֪��Na��K�����ʵ���Ϊ0.075mol��2=0.15mol����Na��K���ʵ����ֱ�Ϊxmol��ymol���������ʵ�����������ʽ���㣻
��3������A��B����ʼû�����壬����һ�����������������壬��������ķ�ӦΪ��HCO3-+H+=H2O+CO2������A��ֻ��Na2CO3����ʼ����CO32-+H+=HCO3-��ǰ������������HCl�������ȣ�ʵ�ʿ�ʼ����������������ڲ���������̼���ĵ������������A���߱���M�е�����ΪNaOH��Na2CO3��B�����У�ǰ��������������֮��Ϊ1��2��������B����M������ΪNa2CO3��NaHCO3���Ҷ������ʵ���֮��Ϊ1��1��
��� �⣺A��B��C�������ڱ��ж�����Ԫ����ɵ����ֳ���������ס��ҡ��������ֵ��ʣ�����B��Ӧ���û���Ӧ���������ǻ��Ϸ�Ӧ��������Ҳ�ǻ��Ϸ�Ӧ�����ʼס����м�Ԫ�صĻ�����A���뻯����B��Ӧ�õ���ͬ�ĵ��ʣ������ֵ��ʷ�Ӧ�ֵõ�������B��Ӧ��Na������������ˮ�ķ�Ӧ������֪����Na���ʣ���Ϊ������B��H2O����Ϊ������C��NaOH��A��Na2O2��
��1�����̪��Һ�м��뻯����Na2O2�ķ�ĩ������������ˮ��Ӧ�����������������������������Ǽ���Һʹ��̪���ɫ�����������ƾ���Ư���ԣ�������Ϊ����Һ�ȱ�����ɫ�������������ɣ�
�ʴ�Ϊ����Һ�ȱ�����ɫ�������������ɣ�
��2�����ʼ��뻯����B��Ӧ�����ӷ���ʽΪ��2Na+2H2O�T2Na++2OH-+H2����
���ݵ���ת���غ��֪��Na��K�����ʵ���Ϊ0.075mol��2=0.15mol����Na��K���ʵ����ֱ�Ϊxmol��ymol��
��x+y=0.15
23x+39y=5.05��
���x=0.05��y=0.1��
�ʺϽ�Ļ�ѧʽΪNaK2��
�ʴ�Ϊ��2Na+2H2O�T2Na++2OH-+H2����NaK2��
��3������A��B����ʼû�����壬����һ�����������������壬��������ķ�ӦΪ��HCO3-+H+=H2O+CO2������A��ֻ��Na2CO3����ʼ����CO32-+H+=HCO3-��ǰ������������HCl�������ȣ�ʵ�ʿ�ʼ����������������ڲ���������̼���ĵ������������A���߱���M�е�����ΪNaOH��Na2CO3��B�����У�ǰ��������������֮��Ϊ1��2��������B����M������ΪNa2CO3��NaHCO3���Ҷ������ʵ���֮��Ϊ1��1��
����Aȷ���μ�ǰ60mL������ʱ��������Ӧ�����ӷ���ʽΪ��OH-+H+=H2O��H++CO32-=HCO3-��
�ʴ�Ϊ��OH-+H+=H2O��H++CO32-=HCO3-��
����Aͼ����������60mL����ʱ��ʼ����������̼����75mLʱ������̼�������������Լ����������60mL��75mLʱ����������̼�����Ʒ�Ӧ�����ݷ�Ӧ�Ĺ�ϵʽ��֪2n��Na2CO3��=n��HCl��������Ӧ��n��HCl������2n��Na2CO3��������ԭ��Һ������ΪNa2CO3��NaOH��
�ʴ�Ϊ��Na2CO3��NaOH��
�ۼ���75mL����ʱ������̼����������ʱ��ҺΪNaCl��Һ������NaԪ���غ㡢�������غ㣬��n��NaOH��=n��HCl��=0.075L��0.1mol/L=0.0075mol������ԭ������NaOH��Һ�����ʵ���Ũ��Ϊ $\frac{0.0075mol}{0.05L}$=0.15mol/L��
�ʴ�Ϊ��0.15mol/L��
������A���ɶ�����̼�����������Ϊ��75-60��mL=15mL������B���ɶ�����̼�����������Ϊ��75-25��mL=50mL����HCO3-+H+=H2O+CO2����֪��������ʵ��ͨ���CO2�����֮��=15mL��50mL=3��10��
�ʴ�Ϊ��3��10��
���� ���⿼�������ƶϡ���ѧ����ȣ��������ڲ²���֤���ƶϣ���Ҫѧ����������Ԫ�ػ�����֪ʶ����3���м���ؼ��Ǹ���ͼ���ж���Һ���ʵijɷ֣���Ŀ�ѶȽϴ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�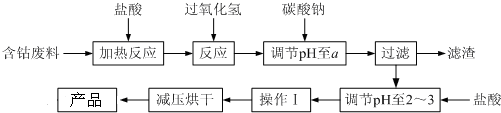
��֪�����������ᷴӦ�Ļ�ѧ����ʽΪ��Co+2HCl=CoCl2+H2��
��CoCl2•6H2O�۵�86�棬������ˮ�����ѵȣ��������ȶ�����������110��120��ʱ��ʧȥ�ᾧˮ����ж�����ˮ�Ȼ��ܣ�
�۲���������������������ʽ����ʱ��Һ��pH���±���
| ������ | Fe��OH��3 | Fe��OH��2 | Co��OH��2 | Al��OH��3 |
| ��ʼ���� | 2.3 | 7.5 | 7.6 | 3.4 |
| ��ȫ���� | 4.1 | 9.7 | 9.2 | 5.2 |
��1���������¹����У��á����ᡱ����ԭ�����С�����������Ļ��ᡱֱ���ܽ⺬�ܷ��ϣ�����Ҫ�ŵ�Ϊ���ٵ�����������ж�������ŷţ���ֹ��Ʒ�л��������Σ�
��2�������������������ǽ�Fe2+������Fe3+��
��3������̼���Ƶ���pH��a��a�ķ�Χ��5.2��7.6��
��4�����������3������ʵ�����������������Ũ������ȴ�ᾧ���ˣ�
��5��Ϊ�ⶨ��Ʒ��CoCl2•6H2O������ijͬѧ��һ��������Ʒ����ˮ���������м���������AgNO3��Һ�����ˣ�����������ɺ������������ͨ�����㷢�ֲ�Ʒ��CoCl2•6H2O��������������100%����ԭ���������Ʒ�к���NaCl���ʣ�����ʱʧȥ�˲��ֽᾧˮ����
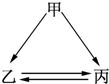 ���и������ʲ���һ��ʵ����ͼת����ϵ���ǣ�������
���и������ʲ���һ��ʵ����ͼת����ϵ���ǣ�������| ���� ��� | �� | �� | �� |
| A | Na | NaOH | NaCl |
| B | AlO3 | Na AlO2 | Al��OH��3 |
| C | CuO | Cu��OH��2 | CuSO4 |
| D | Fe | FeCl3 | FeCl2 |
| A�� | A | B�� | B | C�� | C | D�� | D |
| ���Ӵ��� | �� | �� | �� | �� |
| ������ | 10 | 16 | 18 | 26 |
| A�� | ��������������������������ӻ�Ϊͬ���칹�� | |
| B�� | ��������ͨ��������Ȼ�̼��Һ�У�����ʹ����ɫ | |
| C�� | �����ҵķ��������е�ԭ����ͬһƽ���� | |
| D�� | ������Ͷ��������壬�����ø������������Һ |
| A�� | X�����������������������Ⱦ�Ϊ1��2 | |
| B�� | Y���������۵�ߣ����������²��� | |
| C�� | Z����������������������������κ��ᷴӦ | |
| D�� | R��ͬ�����⻯���ȶ��Դ����������μ��� |
| A�� | HCO3-��������CO32-���� | |
| B�� | ��μ���ϡ���ᣬ�տ�ʼ��������� | |
| C�� | c��Na+��+c��H+��=c��HCO3-��+2c��CO32-��+c��OH-�� | |
| D�� | 2c��Na+��=3[c��HCO3-��+c��CO32-��+c��H2CO3��] |
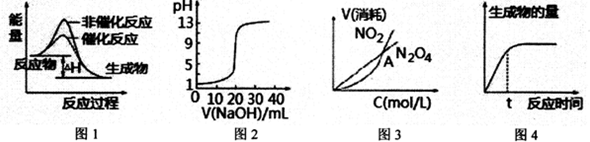
| A�� | ͼl��ʾij���ȷ�Ӧ�ֱ����С�����������·�Ӧ�����е������仯 | |
| B�� | ͼ2��ʾ0.1000mol•L-1NaOH��Һ�ζ�20.00mL0.1 000mol•L-1 CH3COOH��Һ���õ��ĵζ����� | |
| C�� | ͼ3��ʾ���º��������£�2NO2��g��?N2O4��g���У������ʵ�Ũ��������������֮��Ĺ�ϵ�����н���A��Ӧ��״̬Ϊ��ѧƽ��״̬ | |
| D�� | ͼ4��ʾij���淴Ӧ����������淴Ӧʱ��仯�����ߣ���ͼ֪tʱv����v�� |
| A�� | ���ڵ�KOH | B�� | NaCl��Һ | C�� | Һ̬HCl | D�� | MgCl2���� |