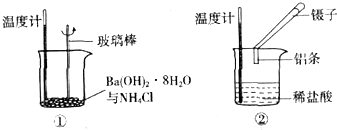
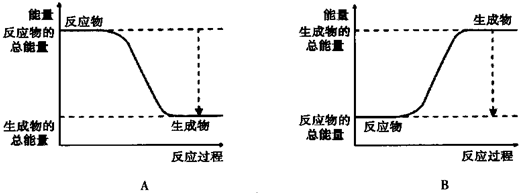
题目内容
16.如图所示为立方烷(cunane)的球棍模型,下列有关说法不正确的是( )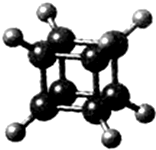
| A. | 它在核磁共振氢谱中只出现一个峰 | |
| B. | 它二氯代物有三种同分异构体 | |
| C. | 它是一种不饱和烃,既能发生取代反应,又能发生加成反应 | |
| D. | 它与苯乙烯(C6H5-CH=CH2)互为同分异构体 |
分析 立方烷整个分子的结构是立方体形,且分子结构是对称的,只有1种氢原子,立方烷二氯代物有3种:两个氯原子在立方体同边有一种情况,两个氯原子的位置在对角有两种情况,所以同分异构体有三种,分子中不含碳碳双键,以此解答.
解答 解:A.立方烷整个分子的结构是立方体形,且分子结构是对称的,只有1种氢原子,故A正确;
B.立方烷二氯代物有三种:两个氯原子在立方体同边有一种情况,两个氯原子的位置在对角有两种情况,所以同分异构体有三种,故B正确;
C.为饱和烃,不含碳碳双键,不能发生加成反应,故C错误;
D.苯乙烯的分子式与立方烷的分子式相同,但结构不同,所以它们互为同分异构体,故D正确.
故选C.
点评 本题考查有机物的结构和性质,为高考常见题型,侧重于学生的分析能力的考查,注意把握有机物的结构和官能团的性质,为解答该类题目的关键,难度不大.

练习册系列答案
相关题目
9.现代炼锌的方法可分为火法和湿法两大类.火法炼锌是将闪锌矿(主要含ZnS)焙烧使它转化为氧化锌,再把氧化锌和焦炭混合,在鼓风炉中加热至1100℃~1300℃,使锌蒸馏出来(设空气中N2、O2的体积分数分别为0.80、0.20),主要反应为:
焙烧炉中:2ZnS(s)+3O2(g)→2ZnO(s)+2SO2(g) ①
鼓风炉中:2C(s)+O2(g)→2CO ②
鼓风炉中:ZnO(s)+CO(g)?Zn(g)+CO2(g) ③
(1)已知闪锌矿中含硫的质量分数为16.0%,而所含杂质不含硫,则闪锌矿中硫化锌的质量分数为48.5%.现代工业生产多采用联合生产,可将闪锌矿中的硫用于生产硫酸.现有
此闪锌矿100t,在理论上可生产出98.0%的硫酸50t.
(2)焙烧炉产生的炉气中SO2的体积分数不超过14.3%(保留小数点后一位小数,下同).
(3)鼓风炉容积固定,炉内部分气态物质其物质的量浓度(mol/L)变化如下:
则鼓风炉中CO总的转化率为90.9%;若生产中CO总的利用率为95.0%,列式计算每生产1molZn,至少需要补充焦炭多少克?
(4)若ZnS全部转化为Zn,焙烧炉出来的N2、O2、SO2混合气体中N2占82.5%,鼓风炉中CO的转化率为62.5%,而O2无剩余,试列式计算每生产1mol Zn,应向焙烧炉和鼓风炉中鼓入新鲜空气共多少升(S.T.P)?
焙烧炉中:2ZnS(s)+3O2(g)→2ZnO(s)+2SO2(g) ①
鼓风炉中:2C(s)+O2(g)→2CO ②
鼓风炉中:ZnO(s)+CO(g)?Zn(g)+CO2(g) ③
(1)已知闪锌矿中含硫的质量分数为16.0%,而所含杂质不含硫,则闪锌矿中硫化锌的质量分数为48.5%.现代工业生产多采用联合生产,可将闪锌矿中的硫用于生产硫酸.现有
此闪锌矿100t,在理论上可生产出98.0%的硫酸50t.
(2)焙烧炉产生的炉气中SO2的体积分数不超过14.3%(保留小数点后一位小数,下同).
(3)鼓风炉容积固定,炉内部分气态物质其物质的量浓度(mol/L)变化如下:
| 时间/min | CO | Zn | CO2 |
| 0 | 0.11 | 0 | 0 |
| 2 | 0.10 | 0.01 | 0.01 |
| 3 | 0.01 | 0.10 | 0.10 |
| 4 | 0.01 | 0.10 | 0.10 |
(4)若ZnS全部转化为Zn,焙烧炉出来的N2、O2、SO2混合气体中N2占82.5%,鼓风炉中CO的转化率为62.5%,而O2无剩余,试列式计算每生产1mol Zn,应向焙烧炉和鼓风炉中鼓入新鲜空气共多少升(S.T.P)?
11.浓氨水可与新制生石灰作用生成氨气,干燥的氨气在高温下能被CuO氧化成N2实验室欲用图仪器装置和药品来制取纯净的氮气.
试回答下列问题:
(1)这些装置按气流方向自左向右的连接顺序是(填A、B、C…)F→G→H→A→B→D→C(A、B顺序可颠倒).
(2)E中发生反应的化学方程式是CaO+NH3•H2O=Ca(OH)2+NH3↑.
(3)装置④中应当选用的干燥剂是(写名称)碱石灰.
(4)装置①中发生氧化还原反应的化学方程式是2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$N2↑3H2O+3Cu.其中氧化剂是CuO,氧化产物是N2(写化学式).
(5)装置②中浓硫酸的作用是除去水蒸气和氨气.
| 序号 | ① | ② | ③ | ④ |
| 仪器装置 | 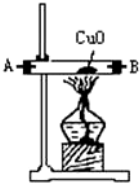 | 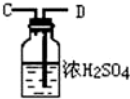 | 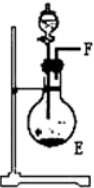 |  |
(1)这些装置按气流方向自左向右的连接顺序是(填A、B、C…)F→G→H→A→B→D→C(A、B顺序可颠倒).
(2)E中发生反应的化学方程式是CaO+NH3•H2O=Ca(OH)2+NH3↑.
(3)装置④中应当选用的干燥剂是(写名称)碱石灰.
(4)装置①中发生氧化还原反应的化学方程式是2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$N2↑3H2O+3Cu.其中氧化剂是CuO,氧化产物是N2(写化学式).
(5)装置②中浓硫酸的作用是除去水蒸气和氨气.
1.下列分子或离子之间互为等电子体的是( )
| A. | CS2和NO2 | B. | N2和CO | C. | CO2和SO2 | D. | NH3和NH4+ |
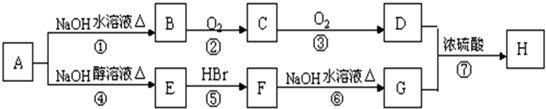
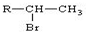 (R为烃基)
(R为烃基)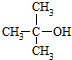 .
.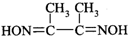 是检验Ni2+的灵敏试剂.
是检验Ni2+的灵敏试剂.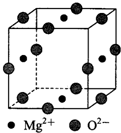
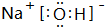 ,CB2的电子式为
,CB2的电子式为 .
.