题目内容
5.某实验小组同学进行如下实验,以探究化学反应中的能量变化.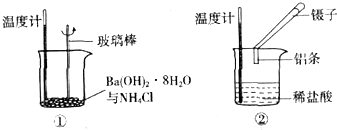
(1)实验表明:①中的温度降低,由此判断氢氧化钡晶体与氯化铵晶体反应是吸热(填“吸热”或“放热”)反应,且反应物能量生成物能量(填“大于”、“小于”、”等于”);
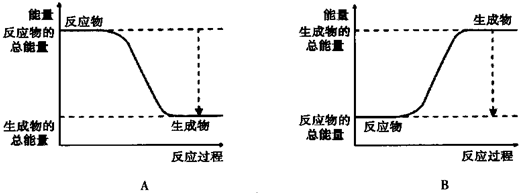
(2)②实验中,该小组同学在烧杯中加入盐酸,再放入用砂纸打磨过的铝条,该反应是放热(填“吸热”或“放热”)反应,离子反应方程式2Al+6H+=2Al3++3H2↑,其能量变化可用如图中的A(填“A”或“B”)表示.
分析 (1)温度升高,则反应放热;温度降低则反应吸热;吸热反应中,反应物的总能量小于生成物的总能量;
(2)金属与酸反应产生氢气的反应是放热反应;放热反应中,反应物的总能量大于生成物的总能量,根据金属与酸的反应为放热反应分析.
解答 解:(1)①中的温度降低,由此判断氢氧化钡晶体与氯化铵晶体反应是吸热反应,吸热反应中,反应物的总能量小于生成物的总能量;
故答案为:吸热,小于;
(2)金属与酸反应产生氢气的反应是放热反应,所以铝与盐酸的反应放热,反应实质是铝与氢离子的反应,生成铝离子和氢气;在放热反应中,反应物的总能量大于生成物的总能量,其能量变化可用如图A表示;
故答案为:放热,2Al+6H+=2Al3++3H2↑,A.
点评 此题是一道实验探究题,解题的关键是分析实验的过程,并结合题中所给的信息结合所学相关知识对问题进行探讨与分析.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.X、Y、Z均为短周期主族元素,已知它们的原子序数的关系为 X+Z=2Y,且Z的最高价氧化物对应的水化物是强酸.则下列有关说法中正确的是( )
| A. | 若X是Na,则Z 的最高价一定为偶数 | |
| B. | 若X是O,则YX一定是离子化合物 | |
| C. | 若Y是O,则非金属性:Z>Y>X | |
| D. | 若Y是Na,则X Z不可能是同一主族元素 |
16.如图所示为立方烷(cunane)的球棍模型,下列有关说法不正确的是( )
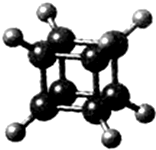

| A. | 它在核磁共振氢谱中只出现一个峰 | |
| B. | 它二氯代物有三种同分异构体 | |
| C. | 它是一种不饱和烃,既能发生取代反应,又能发生加成反应 | |
| D. | 它与苯乙烯(C6H5-CH=CH2)互为同分异构体 |
17.下列实验操作或原理中,正确的是( )
| A. | 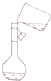 定容 | B. | 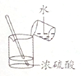 稀释浓硫酸 | C. | 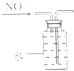 排水法收集NO | D. |  实验室制氨气 |
14.用价层电子对互斥理论预测SO2和NO3-的立体结构,两个结论都正确的是( )
| A. | 直线形;三角锥形 | B. | V形;三角锥形 | ||
| C. | 直线形;平面三角形 | D. | V形;平面三角形 |
15.由石英砂(主要含SiO2)制取高纯硅的工业流程如下:下列说法不正确的是( )

| A. | 反应①③均属于置换反应 | |
| B. | 反应①中氧化产物和还原产物的质量比为1:2 | |
| C. | 该流程中反应①③的还原剂不能互换使用 | |
| D. | 该流程是实现半导体工业“从沙滩到用户”的基础 |
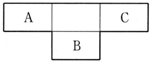 A、B、C为短周期元素,在周期表中所处的位置关系如图所示.A、C两元素的原子核外电子数之和等于B原子的质子数.B原子核内质子数和中子数相等.
A、B、C为短周期元素,在周期表中所处的位置关系如图所示.A、C两元素的原子核外电子数之和等于B原子的质子数.B原子核内质子数和中子数相等.