��Ŀ����
6��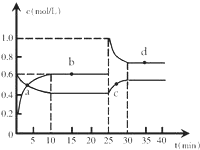 �ں��º��������£���һ����NO2��N2O4�Ļ������ͨ���ݻ�Ϊ2L���ܱ������з�����Ӧ��N2O4 ��g��?2NO2 ��g����H��0����Ӧ�����и����ʵ����ʵ���Ũ��c��ʱ��t�ı仯��ϵ��ͼ��ʾ��
�ں��º��������£���һ����NO2��N2O4�Ļ������ͨ���ݻ�Ϊ2L���ܱ������з�����Ӧ��N2O4 ��g��?2NO2 ��g����H��0����Ӧ�����и����ʵ����ʵ���Ũ��c��ʱ��t�ı仯��ϵ��ͼ��ʾ����1�����¶�ʱ���÷�Ӧ��ƽ�ⳣ��Ϊ0.9��
��2��a��b��c��d�ĸ����У���ѧ��Ӧ����ƽ��״̬����b��d�㣮
��3��25minʱ��������0.8molmolNO2�������ʵĻ�ѧʽ��ʹƽ�ⷢ�����ƶ���
��4��d���ӦNO2�����ʵ���Ũ�ȣ������������������=����0.8mol•L-1��������NO2�����ʵ���Ũ��Ϊ0.8mol•L-1ʱ��Q=1.28������K����ӦӦ����������У���һ������NO2�����ʵ���Ũ�ȣ�
���� ��1������ͼ�е����ݼ����ƽ��ʱ�����ʵ�Ũ�ȣ��ټ���ƽ�ⳣ����
��2������ͼ�����ʵ�Ũ�Ȳ������仯ʱ��ʾ��ѧ��Ӧ����ƽ��״̬��
��3��c��NO2��˲������ƽ��״̬�����ˣ�1-0.6����2=0.8mol��
��4������ƽ��ʱ����������Ũ��Ϊ0.8mol•L-1������Qc=$\frac{{c}^{2}��N{O}_{2}��}{c��{N}_{2}{O}_{4}��}$��K�Ĺ�ϵ�жϣ�
��� �⣺��1������ͼ��֪��ƽ��ʱc��NO2��=0.6mol•L-1��c��N2O4��=0.4mol•L-1���ʸ��¶��¸÷�Ӧ��ƽ�ⳣ��K=$\frac{0��{6}^{2}}{0.4}$=0.9��
�ʴ�Ϊ��0.9��
��2����ͼ��֪��10-25min��30min֮������ʵ����ʵ���Ũ�Ȳ������仯������Ӧʱ����ڵĵ㴦�ڻ�ѧƽ��״̬����b��d���ڻ�ѧƽ��״̬��
�ʴ�Ϊ��b��d��
��3������25min������ʵ�Ũ�ȱ仯��֪��25minʱ������NO2�����������ʵ���=��1.0mol•L-1-0.6mol•L-1����2L=0.8mol��
�ʴ�Ϊ��0.8mol�� NO2��
��4������ƽ��ʱ����������Ũ��Ϊ0.8mol•L-1�����ʱQc=$\frac{{c}^{2}��N{O}_{2}��}{c��{N}_{2}{O}_{4}��}$=$\frac{0��{8}^{2}}{0.5}$=1.28��K=0.9����ƽ��Ҫ���淽���ƶ���ʹ����������Ũ�Ƚ��ͣ�����ƽ��ʱ����������Ũ��С��0.8mol•L-1��
�ʴ�Ϊ������NO2�����ʵ���Ũ��Ϊ0.8 mol•L-1ʱ��Q=1.28������K����ӦӦ����������У���һ������NO2�����ʵ���Ũ�ȣ�
���� ���⿼�黯ѧ��Ӧ���ʼ���ѧƽ��ͼ����Ҫ�漰��Ӧ���ʵļ��㡢Ӱ��ƽ������ء�K�ļ��㼰Ӧ�õȣ���ȷͼ�����ݺ����꼰�㡢�ߡ���������ǽ����Ĺؼ�����Ŀ�Ѷ��еȣ�

| A�� | CaCl2$\stackrel{CO_{2}}{��}$CaCO3$\stackrel{����}{��}$CaO | B�� | Fe$\stackrel{����Cl_{2}}{��}$FeCl2$\stackrel{NaOH��Һ}{��}$Fe��OH��2 | ||
| C�� | Al2O3$\stackrel{NaOH��Һ}{��}$NaAlO2$\stackrel{CO_{2}}{��}$Al��OH��3 | D�� | SiO2$\stackrel{ˮ}{��}$H2SiO3$\stackrel{NaOH��Һ}{��}$Na2SiO3 |
ʱ��s Ũ��mol/L | 0 | 20 | 40 | 60 | 80 | 100 |
| c��N2O4�� | 0.100 | c1 | 0.050 | c3 | a | b |
| c��NO2�� | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
��1���÷�Ӧ�ﵽƽ��ʱ��������������ת����Ϊ60%������c2��c3�����������������=������
��2��20sʱ������������Ũ��c1=0.070mol/L����0s��20sʱ����ڣ�������������ƽ����Ӧ����Ϊ0.0015mol/��L•s����
��3��100��ʱ���÷�Ӧ��ƽ�ⳣ��K=0.36mol/L��
��4��������ͬ����������������г�����Ƕ����������壬Ҫ�ﵽ����ͬ����ƽ��״̬��������������ʼŨ����0.200mol/L��
��5��������ͬ�������������г���0.2mol������������0.3mol�����������壬��ƽ��ǰv�������� v���棩�����������������=������




 �������������ǵĽ���ϢϢ��أ�Ŀǰ�ҹ�ͨ�����6����Ⱦ�������Ũ���������������ָ����AQI����SO2��NO2��CO������3���е���Ⱦ�
�������������ǵĽ���ϢϢ��أ�Ŀǰ�ҹ�ͨ�����6����Ⱦ�������Ũ���������������ָ����AQI����SO2��NO2��CO������3���е���Ⱦ�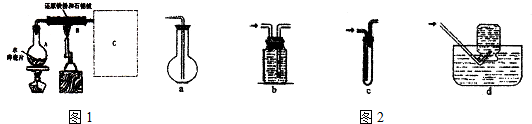
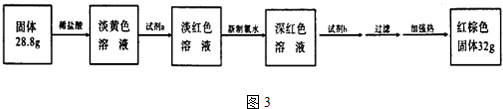
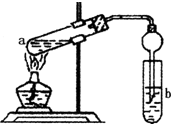 ��ͼ�������Թ����ȼ���2mL 95%���Ҵ�������ҡ���»�������3mLŨ���ᣬ�ټ���2mL���ᣬ���ҡ�ȣ������Թ��м���5mL����Na2CO3��Һ����ͼ���Ӻ�װ�ã��þƾ��ƶ����Թ�С�����3��5min���ô����ȣ����۲쵽���Թ�������������ʱֹͣʵ�飮
��ͼ�������Թ����ȼ���2mL 95%���Ҵ�������ҡ���»�������3mLŨ���ᣬ�ټ���2mL���ᣬ���ҡ�ȣ������Թ��м���5mL����Na2CO3��Һ����ͼ���Ӻ�װ�ã��þƾ��ƶ����Թ�С�����3��5min���ô����ȣ����۲쵽���Թ�������������ʱֹͣʵ�飮