题目内容
15.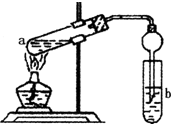 如图,在左试管中先加入2mL 95%的乙醇,并在摇动下缓缓加入3mL浓硫酸,再加入2mL乙酸,充分摇匀.在右试管中加入5mL饱和Na2CO3溶液.按图连接好装置,用酒精灯对左试管小火加热3~5min后,改用大火加热,当观察到右试管中有明显现象时停止实验.
如图,在左试管中先加入2mL 95%的乙醇,并在摇动下缓缓加入3mL浓硫酸,再加入2mL乙酸,充分摇匀.在右试管中加入5mL饱和Na2CO3溶液.按图连接好装置,用酒精灯对左试管小火加热3~5min后,改用大火加热,当观察到右试管中有明显现象时停止实验.(1)写出a试管中主要反应的方程式CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O;
(2)试管b中观察到的主要现象是溶液分层、油状液体在上层;
(3)加入浓硫酸的作用:催化剂和吸水剂;
(4)饱和Na2CO3的作用是:吸取乙醇、除去乙酸,降低乙酸乙酯的溶解度;
(5)在实验中球形干燥管除起冷凝作用外,另一个重要作用是防止倒吸;
(6)反应开始时用酒精灯对左试管小火加热的原因是:加快反应速率,同时防止反应物为来得及反应而挥发损失;(已知乙酸乙酯的沸点为77℃;乙醇的沸点为78.5℃;乙酸的沸点为117.9℃)后改用大火加热的目的是蒸出生成的乙酸乙酯,使可逆反应向右进行.
(7)分离右试管中所得乙酸乙酯和Na2CO3溶液的操作为(只填名称)分液,所需主要仪器为分液漏斗.
分析 (1)a试管中乙醇和乙酸发生酯化反应生成乙酸乙酯和水;
(2)b中为碳酸钠溶液,与乙酸乙酯分层,且乙酸乙酯的密度比水的密度小;
(3)酯化反应为可逆反应,且浓硫酸吸收水,利用反应正向移动;
(4)饱和碳酸钠溶液可吸取乙醇、除去乙酸,降低乙酸乙酯的溶解度;
(5)球形干燥管除起冷凝作用外,可防止倒吸;
(6)先小火加热防止乙酸、乙醇挥发,改用大火加热根据反应为可逆反应及时蒸出生成的乙酸乙酯,使反应向右进行;
(7)乙酸乙酯和Na2CO3溶液分层.
解答 解:(1)醋酸和乙醇在浓硫酸催化作用下发生酯化反应,生成乙酸乙酯和水,反应的化学方程式为CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O,
故答案为:CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O;
(2)b中为碳酸钠溶液,与乙酸乙酯分层,且乙酸乙酯的密度比水的密度小,试管b中观察到的主要现象是溶液分层、油状液体在上层,
故答案为:溶液分层、油状液体在上层;
(3)酯化反应为可逆反应,且浓硫酸吸收水,利用反应正向移动,则该反应为浓硫酸的作用为催化剂和吸水剂,
故答案为:催化剂和吸水剂;
(4)饱和碳酸钠溶液的作用为吸取乙醇、除去乙酸,降低乙酸乙酯的溶解度,偏于分层,
故答案为:吸取乙醇、除去乙酸,降低乙酸乙酯的溶解度;
(5)乙醇、乙酸易溶于水,则球形干燥管除起冷凝作用外,另一个重要作用是防止倒吸,
故答案为:防止倒吸;
(6)本实验反应开始时用小火加热,目的是加快反应速率,同时由于反应物乙酸、乙醇沸点较低,小火加热防止反应物为来得及反应而挥发损失,后改用大火加热,只因为反应为可逆反应,及时蒸出生成的乙酸乙酯,使反应向右进行.
故答案为:加快反应速率,同时防止反应物为来得及反应而挥发损失;蒸出生成的乙酸乙酯,使可逆反应向右进行;
(7)乙酸乙酯和Na2CO3溶液分层,分液法分离,主要仪器为分液漏斗,故答案为:分液;分液漏斗.
点评 本题考查有机物的制备实验,为高频考点,把握反应原理、实验装置的作用、混合物分离为解答的关键,侧重分析与实验能力的考查,注意(6)中平衡移动的应用,题目难度不大.

 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案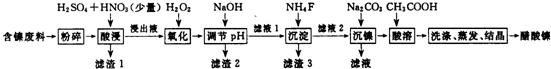
相关离子生成氢氧化物的pH和相关物质的溶解性如下表:
| 表1 | 表2 | |||
| 物质 | 开始沉淀的pH | 沉淀完全的pH | 物质 | 20℃时溶解性(H2O) |
| Fe3+ | 1.1 | 3.2 | CaSO4 | 微溶 |
| Fe2+ | 5.8 | 8.8 | NiF | 可溶 |
| Al3+ | 3.0 | 5.0 | CaF2 | 难溶 |
| Ni2+ | 6.7 | 9.5 | NiCO3 | KSP=9.60×10-6 |
(2)滤渣1和滤渣3主要成分的化学式分别是SiO2、CaSO4、CaF2.
(3)写出氧化步骤中加入H2O2发生反应的离子方程式2Fe2++H2O2+2H+═2Fe3++2H2O.
(4)酸浸过程中,lmol NiS失去6NA个电子,同时生成两种无色有毒气体.写出该反应的化学方程式NiS+H2SO4+2HNO3═NiSO4+SO2↑+2NO↑+2H2O.
(5)沉镍过程中,若c(Ni2+)=2.0mol•L-1,欲使100mL该滤液中的Ni2+沉淀完全[c(Ni2+)≤10-5mol•L-1],则需要加入Na2CO3固体的质量最少为31.4gg.(保留小数点后1位有效数字)
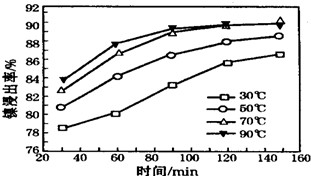
(6)保持其他条件不变,在不同温度下对含镍废料进行酸浸,镍浸出率随时间变化如下图.酸浸的最佳温度与时间分别为70℃、120min.
NaBr+H2SO4═HBr+NaHSO4 ①
R-OH+HBr?R-Br+H2O ②
可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br-被浓硫酸氧化为Br2等.有关数据列表如下;
| 物质 | 乙醇 | 溴乙烷 | 正丁醇 | 1-溴丁烷 |
| 密度/g•cm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
| 沸点/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
(1)在溴乙烷和1-溴丁烷的制备实验中,下列仪器最不可能用到的是d.
a.圆底烧瓶 b量筒. c.锥形瓶 d.容量瓶
(2)溴代烃的水溶性小于(填“大于”、“等于”或“小于”)相应的醇;其原因是醇分子可与水分子形成氢键,溴代烃分子不能与水分子形成氢键.
(3)将1-溴丁烷粗产品置于分液漏斗中加水,振荡后静置,水层在上层(填“上层”、“下层”或“不分层”).
(4)制备操作中,加入的浓硫酸必须进行稀释,其目的不正确的是a.
a.水是反应的催化剂 b.减少Br2的生成
c.减少HBr的挥发 d减少副产物烯和醚的生成
(5)在制备溴乙烷时,采用边反应边蒸出产物的方法,其原因是平衡向生成溴乙烷的方向移动;但在制备1-溴丁烷时却不能边反应边蒸出产物,其原因是1-溴丁烷与正丁醇的沸点差较小,若边反应边蒸馏,会有较多的正丁醇被蒸出.
| 物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
| 沸点/℃ | 65 | 249 | 199.6 |
在圆底烧瓶中加入3mL浓硫酸、12.2g苯甲酸、20mL甲醇(密度约为0.79g/cm3).
(1)液体混合时,正确的加入顺序是先加入12.2g苯甲酸和20mL甲醇,再小心加入3mL浓硫酸.
(2)为防止圆底烧瓶中的液体在实验时发生暴沸,在加热前应采取的措施是加入沸石或碎瓷片.
(3)在该反应中反应物甲醇应过量,其理由是该反应是可逆反应,甲醇比苯甲酸价廉,且甲醇沸点低,易损失,故可增加甲醇的量,以提高苯甲酸的转化率.
Ⅱ.粗产品的精制
(4)现拟用下列流程精制苯甲酸甲酯,请根据流程图填入恰当操作方法的名称:操作1为分液,操作2为蒸馏.
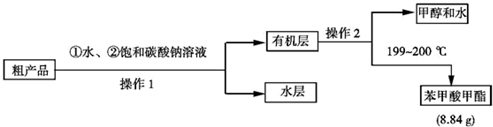
(5)苯甲酸甲酯的产率为65%.
(6)苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,某同学做了如下检验.
| 检验项目 | 实验现象及结论 |
| 检验粗产品中含有水的操作是 | |
| 检验粗产品中含有硫酸的操作是 |
| t/s | 0 | 500 | 1 000 | 1 500 |
| c(N2O5)mol/L | 5.00 | 3.52 | 2.50 | 2.50 |
| A. | 500 s内N2O5分解速率为2.96×10-3 mol/(L•s) | |
| B. | T1温度下的平衡常数为K1=125,1 000 s时转化率为50% | |
| C. | 其他条件不变时,T2温度下反应到1 000 s时测得N2O5(g)浓度为2.98 mol/L,则T1<T2 | |
| D. | T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1>K2 |
| A. | 配制90mL1.00mol/L的NaCl溶液,用托盘天平称取5.3gNaCl固体 | |
| B. | 使用容量瓶时,先检验其是否漏水,然后洗净后,不用干燥即可使用 | |
| C. | 可用10mL量筒量取8.58mL蒸馏水 | |
| D. | 在配制溶液定容后,上下翻转摇匀后发现液面下降,须加水至溶液凹液面与刻度线相切 |

下列说法正确的是( )
| A. | 滤液A中的阳离子为Fe2+、Fe3+、H+ | |
| B. | 该样品中Cu、O元素的质量比为10:l | |
| C. | V=448 | |
| D. | 溶解样品时消耗H2SO4的物质的量为0.04 mo1 |
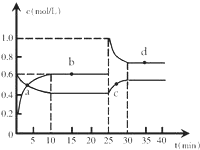 在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中发生反应:N2O4 (g)?2NO2 (g)△H>0,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.
在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中发生反应:N2O4 (g)?2NO2 (g)△H>0,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.