��Ŀ����
4����ϩ��һ����;�㷺�Ļ����л�����ԭ�ϣ����������ϳ�̼���������DMC������Ҫ������Ʒ�����ַ�Ӧ��������ȥ����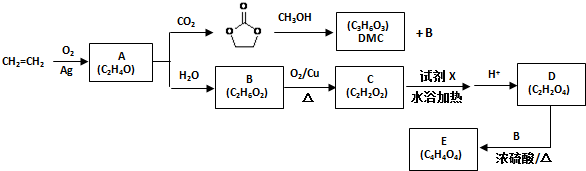
��֪�����ǻ�ֱ����̼̼˫���������ȶ���R-CH=CH-OH��R-CH2-CHO
�ڻ�����A�ĺ˴Ź�������ͼ��ֻ��ʾ1���
��1����ҵ��������ϩ����Ҫ������ʯ���ѽ⣬�Լ�XΪ������Һ��
��2������˵����ȷ����AD
A��D��E�ķ�Ӧ����Ϊȡ����Ӧ
B��������A�뻯����C������ͬ������
C��DMC������������Ϊͬϵ��
D��DMC����������ˮ���ܲ���CO2�ͼ״�
��3��д��д��������C�������Լ�X��Ӧ�Ļ�ѧ����ʽ
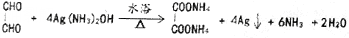 ��
����4���ִ���ҵҲ�������أ�
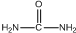 ���ͼ״��ڴ��������������£�����ȡ����Ӧ����DMC����д���÷�Ӧ�Ļ�ѧ��Ӧ����ʽ
���ͼ״��ڴ��������������£�����ȡ����Ӧ����DMC����д���÷�Ӧ�Ļ�ѧ��Ӧ����ʽ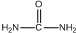 +2CH3OH$��_{��}^{����}$
+2CH3OH$��_{��}^{����}$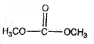 +2NH3����
+2NH3����
���� ��ϩ��������A��������A�ĺ˴Ź�������ͼ��ֻ��ʾ1��壬���A�������̼��Ӧ���� ����֪AΪ
����֪AΪ ��A��ˮ������Ӧ����B����B�ķ���ʽ��֪BΪCH2OHCH2OH��B��������������C�����C�ķ���ʽ��֪CΪOHC-CHO��C����������Ӧ����D����Ӧ��Ҫˮԡ���ȣ����Լ�XΪ������Һ��DΪHOOC-COOH����E�ķ���ʽ��֪�Ҷ������Ҷ�������������Ӧ���ɻ�������EΪ
��A��ˮ������Ӧ����B����B�ķ���ʽ��֪BΪCH2OHCH2OH��B��������������C�����C�ķ���ʽ��֪CΪOHC-CHO��C����������Ӧ����D����Ӧ��Ҫˮԡ���ȣ����Լ�XΪ������Һ��DΪHOOC-COOH����E�ķ���ʽ��֪�Ҷ������Ҷ�������������Ӧ���ɻ�������EΪ ��
�� ��״���Ӧ�õ�DMC���Ҷ��������DMC�ķ���ʽ��֪��DMC�Ľṹ��ʽΪ
��״���Ӧ�õ�DMC���Ҷ��������DMC�ķ���ʽ��֪��DMC�Ľṹ��ʽΪ ��
��
��� �⣺��ϩ��������A��������A�ĺ˴Ź�������ͼ��ֻ��ʾ1��壬���A�������̼��Ӧ���� ����֪AΪ
����֪AΪ ��A��ˮ������Ӧ����B����B�ķ���ʽ��֪BΪCH2OHCH2OH��B��������������C�����C�ķ���ʽ��֪CΪOHC-CHO��C����������Ӧ����D����Ӧ��Ҫˮԡ���ȣ����Լ�XΪ������Һ��DΪHOOC-COOH����E�ķ���ʽ��֪�Ҷ������Ҷ�������������Ӧ���ɻ�������EΪ
��A��ˮ������Ӧ����B����B�ķ���ʽ��֪BΪCH2OHCH2OH��B��������������C�����C�ķ���ʽ��֪CΪOHC-CHO��C����������Ӧ����D����Ӧ��Ҫˮԡ���ȣ����Լ�XΪ������Һ��DΪHOOC-COOH����E�ķ���ʽ��֪�Ҷ������Ҷ�������������Ӧ���ɻ�������EΪ ��
�� ��״���Ӧ�õ�DMC���Ҷ��������DMC�ķ���ʽ��֪��DMC�Ľṹ��ʽΪ
��״���Ӧ�õ�DMC���Ҷ��������DMC�ķ���ʽ��֪��DMC�Ľṹ��ʽΪ ��
��
��1����ҵ��������ϩ����Ҫ������ʯ���ѽ⣬�Լ�XΪ������Һ��
�ʴ�Ϊ��ʯ���ѽ⣻������Һ��
��2��A��D��E�ķ�ӦΪ�����봼��Ũ������������·�����������Ӧ��Ҳ��ȡ����Ӧ����A��ȷ��
B��������AΪ ��������CΪOHCCHO�����Թ����Ų�ͬ����B����
��������CΪOHCCHO�����Թ����Ų�ͬ����B����
C��DMC�Ľṹ��ʽΪ ����������������������Ŀ��ͬ�����Բ���Ϊͬϵ���C����
����������������������Ŀ��ͬ�����Բ���Ϊͬϵ���C����
D��DMC�Ľṹ��ʽΪ ������������ˮ���ܲ���������̼��״�����D��ȷ��
������������ˮ���ܲ���������̼��״�����D��ȷ��
��ѡ��AD��
��3��������C�������Լ�X��Ӧ�Ļ�ѧ����ʽ�� ��
��
�ʴ�Ϊ�� ��
��
��4���������أ� ���ͼ״��ڴ��������������£�����ȡ����Ӧ����DMC����Ӧ�ķ���ʽΪ
���ͼ״��ڴ��������������£�����ȡ����Ӧ����DMC����Ӧ�ķ���ʽΪ +2CH3OH$��_{��}^{����}$
+2CH3OH$��_{��}^{����}$ +2NH3����
+2NH3����
�ʴ�Ϊ�� +2CH3OH$��_{��}^{����}$
+2CH3OH$��_{��}^{����}$ +2NH3����
+2NH3����
���� ���⿼���л�����ƶϣ���������л���Ľṹ�����ʽ����Ӧ�������з����������ڿ���ѧ�����������������ۺ����û�ѧ֪ʶ���������������չ����ŵ�������ת������Ŀ�Ѷ��еȣ�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| A�� | 25��ʱKb��NH3•H2O����10-5 | |
| B�� | �ζ�������ˮ�ĵ���̶�һֱ������������ | |
| C�� | Ϊʹ�յ�����������Կɶ���ϼ��μ��� | |
| D�� | �ζ��յ�ʱc��NH4+��=c��Cl-����c��H+��=c��OH-�� |
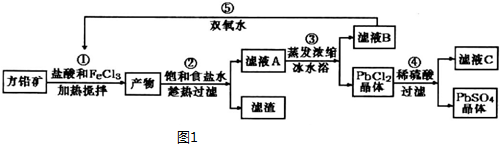
��֪����Ksp��PbSO4��=1.08��10-8��Ksp��PbCl2��=1.6��l0-5��
��PbCl2��s��+2C1-��aq��?PbCl42-��aq����H��0
��Fe3+��Pb2+������������ʽ��ʼ����ʱ��PHֵ�ֱ�Ϊ1.9��7��
��1�������м���������Կ�����Һ��pH��1.9����ҪĿ��������Fe3+��ˮ�⣮
��Ӧ�����пɹ۲쵽����ɫ��������ٶ�Ӧ�����ӷ���ʽΪ2Fe3++PbS=PbCl2+S+2Fe2+��
��2�������õ���ҺA����Ũ�������ñ�ˮԡ��Ŀ�����ñ�ˮԡʹPbCl2��s��+2Cl-��aq��?PbCl4-��H��0�����ƶ���ʹPbCl4-ת��PbCl2����������ƽ���ƶ�ԭ�����ͣ�
��3�����ж�Ӧ��Ӧ��ƽ�ⳣ������ʽ$\frac{{c}^{2}��C{l}^{-}��}{c��S{{O}_{4}}^{2-}��}$��
��4�����������п�ѭ�����õ�������FeCl3��HCl��
��5����Ǧ����Ǧ����ʹˮ�����ؽ���Ǧ�ĺ�����������������Ⱦ��ˮ��Һ��Ǧ�Ĵ�����̬��Ҫ��Pb2+��Pb��OH��+��Pb��OH��2��Pb��OH��3-��Pb��OH��42-������̬��ǦŨ�ȷ���x����ҺpH�仯�Ĺ�ϵ��ͼ2��ʾ��
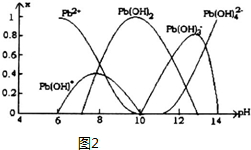
��̽��Pb2+�����ʣ���Pb2+����Һ����εμ�NaOH����Һ����ǣ������μ�NaOH��Һ�ֱ���壻pH��13ʱ����Һ�з�������Ҫ��Ӧ�����ӷ���ʽΪPb��OH��3-+HO-=Pb��OH��42-����
�ڳ�ȥ��Һ�е�Pb2+������С����һ�������Լ���ȥ��ˮ�еĺ���Ǧ�������������ӣ�ʵ������¼���£�
| ���� | Pb2+ | Ca2+ | Fe3+ | Mn2+ |
| ����ǰŨ��/��mg•L-1�� | 0.100 | 29.8 | 0.12 | 0.087 |
| ������Ũ��/��mg•L-1�� | 0.004 | 22.6 | 0.04 | 0.053 |
���������Լ���DH������Ǧ��������Ҫ�����ķ�ӦΪ��2DH��s��+Pb2+?D2Pb��s��+2H+������Ǧʱ����ʵ�pHԼΪ6��
| A�� | ��������ָ����Ԫ�صĻ����� | B�� | ������ᡢ��ζ�����Ԫ�� | ||
| C�� | ����������һ���ǽ��������� | D�� | ����������һ���Ƿǽ��������� |


 ��
��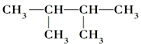
 �����������ԣ���Ka=1.1��10-10��ˮ�����һ�������γɵ�����
�����������ԣ���Ka=1.1��10-10��ˮ�����һ�������γɵ�����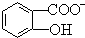 ���γɷ�����������ݴ��жϣ���ͬ�¶��µ���ƽ�ⳣ��Ka2��ˮ���ᣩ��Ka�����ӣ������������������ԭ����
���γɷ�����������ݴ��жϣ���ͬ�¶��µ���ƽ�ⳣ��Ka2��ˮ���ᣩ��Ka�����ӣ������������������ԭ����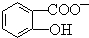 ���γɷ����������ʹ����ѵ����H+��
���γɷ����������ʹ����ѵ����H+��