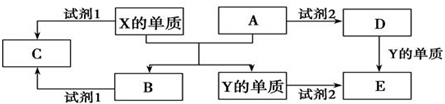
题目内容
10.为检验某溶液中是否含有SO42-、NH4+、Cl-、Fe3+等四种离子,某同学进行了下图所示的实验操作,已知检验过程中产生的气体能使湿润红色石蕊试纸变蓝.由该实验能得到的正确结论是( )
| A. | 原溶液中一定含有SO42- | B. | 原溶液中一定含有NH4+ | ||
| C. | 原溶液中一定含有Cl- | D. | 原溶液中一定含有Fe3+ |
分析 在溶液中加入盐酸酸化的硝酸钡,其中的亚硫酸根离子、亚铁离子会被氧化为硫酸根离子、铁离子,加入的盐酸中含有氯离子,会和硝酸银反应生成氯化银白色沉淀;能使红色石蕊试纸变蓝的气体是氨气,三价铁离子能使硫氰酸钾变为红色,据此进行判断.
解答 解:A.原溶液中加入盐酸酸化的硝酸钡,如果其中含有亚硫酸根离子,则会被氧化为硫酸根离子,所以原溶液中不一定含有SO42-离子,故A错误;
B.产生能使红色石蕊试纸变蓝的气体是氨气,所以原来溶液中一定含有NH4+,故B正确;
C.原溶液中加入盐酸酸化的硝酸钡,引进了氯离子,能和硝酸银反应生成氯化银沉淀的离子不一定是原溶液中含有的氯离子,可能是加进去的盐酸中的,故C错误;
D.原溶液中加入盐酸酸化的硝酸钡,如果其中含有亚铁离子,则亚铁离子会被氧化为铁离子,铁离子能使硫氰酸钾变为红色,所以原溶液中不一定含有Fe3+离子,故D错误;
故选B.
点评 本题考查常见离子的检验方法,题目难度中等,明确常见离子的性质及检验方法为解答关键,注意判断离子是否存在时,需要排除干扰离子,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
1.某原电池结构如图所示,下列有关该原电池的说法正确的是( )
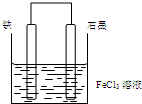

| A. | 电子从石墨棒经外电路流向铁棒 | |
| B. | 总反应为2Fe3++Fe=3 Fe2+ | |
| C. | 石墨电极上发生氧化反应 | |
| D. | 铁电极逐渐变细,石墨电极逐渐变粗 |
18.下列变化中需加入氧化剂才能实现的是( )
| A. | H2S→SO2 | B. | Fe2+→Fe | C. | CO→CO2 | D. | 2H+→H2 |
5.化学实验时应强化安全意识.下列做法正确的是( )
| A. | 金属钠着火时使用泡沫灭火器灭火 | |
| B. | 加热碳酸氢钠固体时,试管管口倾斜向上 | |
| C. | 实验室制取氯气时,用NaOH溶液进行尾气吸收 | |
| D. | 浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗 |
2.将Cu片放入0.1mol•L-1FeCl3溶液中,反应一定时间后取出Cu片,溶液中的C(Fe3+):C(Fe2+)=2:3,则Cu2+与Fe3+的物质的量之比为( )
| A. | 5:3 | B. | 4:3 | C. | 3:4 | D. | 3:5 |
19.下列离子方程式中正确的是( )
| A. | 向NaSiO3溶液中通入过量SO2:SiO32-+SO2+H2O═H2SiO3↓+SO32- | |
| B. | 向稀硝酸中加入少量铁粉:3Fe+8H++2NO3-═3Fe3++2NO↑+4H2O | |
| C. | 碳酸钠的水解:CO32-+2H2O?H2CO3+2OH- | |
| D. | 氢氧化铁溶于氢碘酸:2Fe(OH)3+6H++2I-═2Fe2++I2+6H2O |
20.下列关于有机物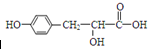 的说法中,正确的是( )
的说法中,正确的是( )
 的说法中,正确的是( )
的说法中,正确的是( )| A. | 在核磁共振氢谱中有五组吸收峰 | |
| B. | 与 互为同分异构体 互为同分异构体 | |
| C. | 1mol 该有机物与NaOH溶液反应,最多消耗3mol NaOH | |
| D. | 可以发生取代反应、加成反应、消去反应和缩聚反应 |
 某课外小组分别用图所示装置对原电池和电解池原理进行实验探究.
某课外小组分别用图所示装置对原电池和电解池原理进行实验探究.