题目内容
20. 某课外小组分别用图所示装置对原电池和电解池原理进行实验探究.
某课外小组分别用图所示装置对原电池和电解池原理进行实验探究.请回答:
Ⅰ.用图1、2所示装置进行第一组实验CH4-8e-+10OH-=CO32-+7H2O.
(1)A极发生反应的电极反应式为CH4-8e-+10OH-=CO32-+7H2O.
(2)N极发生反应的电极反应式为2H++2e-=H2↑.
(3)滤纸上能观察到的现象有滤纸上有红褐色斑点产生.
(4)标准状况11.2L CH4反应则图2可收集气体44.8L(标况)
Ⅱ.用图3所示装置进行第二组实验.实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清.查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色.
(5)电解过程中,X极区溶液的pH增大(填“增大”“减小”或“不变”).
(6)电解过程中,Y极发生的电极反应为Fe-6e-+8OH-═FeO42-+4H2O和4OH--4e-═2H2O+O2↑.
(7)若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少0.28 g.
(8)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为:2K2FeO4+3Zn═Fe2O3+ZnO+2K2ZnO2该电池正极发生的反应的电极反应式为2FeO42ˉ+6eˉ+5H2O=Fe2O3+10OHˉ.
分析 Ⅰ.(1)A是原电池的负极,发生氧化反应,电极发生反应的电极反应式为CH4-8e-+10OH-=CO32-+7H2O;
(2)N极与电源的负极相连是电解池的阴极,发生还原反应,所以电极反应式为2H++2e-=H2↑;
(3)图2中阳极铁失去电子变成亚铁离子,亚铁离子与氢氧根离子结合成氢氧化亚铁,氢氧化亚铁迅速被氧化成红褐色沉淀氢氧化铁沉淀;
(4)根据整个过程转移电子数相等,分析解答;
(5)电解过程中,阴极上氢离子放电生成氢气,则阴极附近氢氧根离子浓度大于氢离子溶液,溶液呈碱性;
(6)铁是活泼金属,电解池工作时,阳极上铁失电子发生氧化反应,氢氧根离子失电子发生氧化反应,所以发生的电极反应式为:Fe-6e-+8OH-═FeO42-+4H2O和4OH--4e-═2H2O+O2;
(7)X电极上析出的是氢气,Y电极上析出的是氧气,且Y电极失电子进入溶液,设铁质量减少为xg,根据转移电子数相等得$\frac{0.672L}{22.4L/mol}$×2=$\frac{0.168L}{22.4L/mol}$×4+
$\frac{xg}{56g/mol}$×6;
(8)在碱性锌电池中,锌做负极发生氧化反应,K2FeO4在正极发生还原反应生成氧化铁,据此书写电极反应式,注意电解质溶液为碱性溶液.
解答 解:Ⅰ.(1)A是原电池的负极,发生氧化反应,电极发生反应的电极反应式为CH4-8e-+10OH-=CO32-+7H2O,故答案为:CH4-8e-+10OH-=CO32-+7H2O;(1)A
(2)N极与电源的负极相连是电解池的阴极,发生还原反应,所以电极反应式为2H++2e-=H2↑,故答案为:2H++2e-=H2↑;
(3)图2中阳极铁失去电子变成亚铁离子,亚铁离子与氢氧根离子结合成氢氧化亚铁,氢氧化亚铁迅速被氧化成红褐色沉淀氢氧化铁沉淀,故答案为:滤纸上有红褐色斑点产生;
(4)根据转移电子数相等可得:CH4~8e-~4H2,
1 4
11.2L 44.8L
故答案为:44.8L;
(5)电解过程中,阴极上氢离子放电生成氢气,则阴极附近氢氧根离子浓度大于氢离子溶液,溶液呈碱性,溶液的pH增大,故答案为:增大;
(6)铁是活泼金属,电解池工作时,阳极上铁失电子发生氧化反应,氢氧根离子失电子发生氧化反应,所以发生的电极反应式为:Fe-6e-+8OH-═FeO42-+4H2O和4OH--4e-═2H2O+O2↑,故答案为:4OH--4e-═2H2O+O2↑;
(7)X电极上析出的是氢气,Y电极上析出的是氧气,且Y电极失电子进入溶液,设铁质量减少为xg,根据转移电子数相等得$\frac{0.672L}{22.4L/mol}$×2=$\frac{0.168L}{22.4L/mol}$×4+
$\frac{xg}{56g/mol}$×6,解得x=0.28g,故答案为:0.28;
(8)在碱性锌电池中,锌做负极发生氧化反应,K2FeO4在正极发生还原反应生成氧化铁,正极的电极反应式为2FeO42ˉ+6eˉ+5H2O=Fe2O3+10OHˉ,
故答案为:2FeO42ˉ+6eˉ+5H2O=Fe2O3+10OHˉ.
点评 本题考查了原电池和电解池原理,为高频考点,侧重于学生的分析能力的考查,注意电解池中如果活泼金属作阳极,则电解池工作时阳极材料失电子发生氧化反应,为易错点,难度中等;

 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案还原法在酸性介质中用FeSO4等将+6价铬还原成+3价铬. 具体流程如下:

有关离子完全沉淀的pH如下表:
| 有关离子 | Fe2+ | Fe3+ | Cr3+ |
| 完全沉淀为对应氢氧化物的pH | 9.0 | 3.2 | 5.6 |
(2)在含铬废水中加入FeSO4,再调节pH,使Fe3+和Cr3+产生氢氧化物沉淀.
则在操作②中可用于调节溶液pH的试剂最好为:BD(填序号);
A.Na2O2B.Ca(OH)2C.Ba(OH)2D.NaOH
此时调节溶液的pH范围在C(填序号)最佳.
A.12~14B.10~11C.6~8D.3~4
(3)将等体积的4.0×10-3mol•L-1的AgNO3和4.0×10-3mol•L-1的K2CrO4溶液混合能析出Ag2CrO4沉淀(Ksp(Ag2CrO4)=9.0×10-12),请写出表示Ag2CrO4溶解平衡的方程式,并简要写出能生成Ag2CrO4沉淀原因的计算过程.
| A. | 0.2 mol•L-1CH3COONa溶液和0.1 mol•L-1HCl溶液等体积混合后:c(CH3COO-)>c(Na+)>c(Cl-)>c(H+)>c(OH-) | |
| B. | pH=3的盐酸和NaOH的混合溶液中:c(Na+)=c(Cl-) | |
| C. | 0.1 mol•L-1NaHCO3 溶液中:c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) | |
| D. | 含SO42-、NH4+、H+、OH-的溶液中可能存在:c(H+)>c(SO42-)>c(NH4+)>c(OH-) |
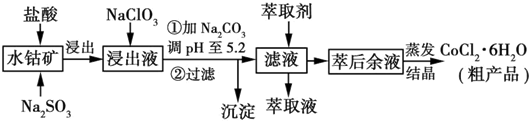
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等:
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(2)NaClO3的作用是将Fe2+氧化成Fe3+.
(3)加Na2CO3调pH至5.2所得沉淀为Fe(OH)3、Al(OH)3.
(4)萃取剂对金属离子的萃取率与pH的关系如图所示.萃取剂的作用是除去溶液中的Mn2+;其使用的适宜pH范围是B(填字母).
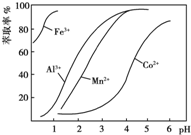
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5
(5)为测定粗产品中CoCl2•6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去部分结晶水(任答一条即可).
| A. | 配制100mL2mol/LNaCl溶液,将称量的NaCl放入烧杯中加20-30mL的蒸馏水搅拌溶解 | |
| B. | 蒸馏操作时,应将温度计插入烧瓶中的溶液中 | |
| C. | 测溶液的pH时,将pH试纸放入溶液中观察其颜色变化,跟标准比色卡比较 | |
| D. | 分液操作时,先将分液漏斗中的下层液体放出,然后再将上层液体放出 |
| A. | 氢氧化钠溶液 | B. | 通入二氧化碳 | C. | 氢氧化钙溶液 | D. | 盐酸 |

| A. | 原溶液中一定含有SO42- | B. | 原溶液中一定含有NH4+ | ||
| C. | 原溶液中一定含有Cl- | D. | 原溶液中一定含有Fe3+ |