题目内容
如图为水果电池的示意图,下列说法正确的是( )


| A、锌片作负极,质量逐渐减少 |
| B、电子由铜片沿导线流向锌片 |
| C、铜电极逐渐溶解 |
| D、该装置能将电能转化为化学能 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:根据金属的活泼性知,Zn作负极,Cu作正极,负极上Zn失电子发生氧化反应,正极上氢离子得电子发生还原反应,电子从负极沿导线流向正极,据此解答.
解答:
解:A、根据金属的活泼性知,Zn作负极,发生氧化反应质量减少,故A正确;
B、电子从负极沿导线流向正极,故B错误;
C、Cu作正极,正极上氢离子得电子发生还原反应,故C错误;
D、该装置能将化学能转化为电能,故D错误;
故选A.
B、电子从负极沿导线流向正极,故B错误;
C、Cu作正极,正极上氢离子得电子发生还原反应,故C错误;
D、该装置能将化学能转化为电能,故D错误;
故选A.
点评:本题考查了原电池原理,为高频考点,侧重于学生的分析能力的考查,难度不大,明确电子的移动方向、电极的判断是解题的关键.

练习册系列答案
相关题目
下列四组实验中,操作正确且能达到预期目的是( )
A、 配制稀硫酸 |
B、 固体NaHCO3分解 固体NaHCO3分解 |
C、 制备Fe(OH)2沉淀 |
D、 收集NH3 |
下列关于实验室制乙烯的说法中,错误的是( )
| A、反应温度必须控制在170℃ |
| B、反应物是乙醇和过量的3mol/L硫酸的混合液 |
| C、温度计应插入反应溶液液面以下 |
| D、反应容器中应加入少许瓷片 |
下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
| A、在NaHA溶液中一定有:c(Na+)>c(HA-)>c(OH-)>c(H+) |
| B、0.1mol/L(NH4)2Fe(SO4)2溶液中:c(SO42-)=c(NH4+)>c(Fe2+)>c(H+)>c(OH-) |
| C、0.2 mol?L-1CH3COOH溶液和0.2 mol?L-1CH3COONa溶液等体积混合:c(CH3COO-)+c(OH-)-c(H+)=0.1 mol?L-1 |
| D、pH相等的①NH4Cl ②(NH4)2SO4③NH4HSO4溶液中,c (NH4+)大小顺序为①=②>③ |
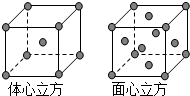 利用有关知识回答下列问题:
利用有关知识回答下列问题: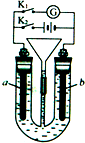 在如图所示装置中,U形管内装满稀H2SO4,a为铁电极,b为多孔石墨电极.
在如图所示装置中,U形管内装满稀H2SO4,a为铁电极,b为多孔石墨电极.
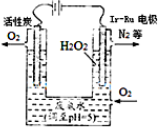 最近华南理工大提出利用电解法制H2O2并用产生的H2O2处理废氨水,装置如图
最近华南理工大提出利用电解法制H2O2并用产生的H2O2处理废氨水,装置如图