题目内容
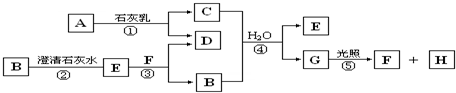
如图中A~H均为中学化学中常见的物质,A、B、H是气体,它们之间有如下转化关系.(反应中生成的水已略去)请回答以下问题:
(1)E是 ,F是 ,H是 .(填化学式)
(2)①-⑤中属于氧化还原反应的有 .
(3)写出反应①的化学反应方程式并用双线桥法标出电子转移的方向和数目: .

(1)E是
(2)①-⑤中属于氧化还原反应的有
(3)写出反应①的化学反应方程式并用双线桥法标出电子转移的方向和数目:
考点:无机物的推断
专题:推断题
分析:G能见光分解,结合反应①和反应④,可判断G为HClO,根据反应②、反应③可推知,B可与澄清石灰水反应生成E还能和次氯酸分解后的产物F反应,应为CO2,则E为CaCO3,F为HCl,D为CaCl2,常见能与石灰水反应的气体还有氯气,则A应为Cl2,由此可知C为Ca(ClO)2,H为O2,据此答题.
解答:
解:G能见光分解,结合反应①和反应④,可判断G为HClO,根据反应②、反应③可推知,B可与澄清石灰水反应生成E还能和次氯酸分解后的产物F反应,应为CO2,则E为CaCO3,F为HCl,D为CaCl2,常见能与石灰水反应的气体还有氯气,则A应为Cl2,由此可知C为Ca(ClO)2,H为O2,
(1)根据上面的分析可知,E是 CaCO3,F是 HCl,H是 O2,
故答案为:CaCO3;HCl;O2;
(2)反应①是氯与氢氧化钙反应,是氯气的自身氧化还原,反应②是复分解反应,反应③是碳酸钙与盐酸反应也是复分解反应,反应④是二氧化碳、水、次氯酸钙反应生成次氯酸,是复分解反应,反应⑤是次氯酸分解,是氧化还反应,所以属于氧化还原反应的有①⑤,
故答案为:①⑤;
(3)反应①的化学方程式(并用双线桥法注明电子得失情况)为: ,
,
故答案为: ;
;
(1)根据上面的分析可知,E是 CaCO3,F是 HCl,H是 O2,
故答案为:CaCO3;HCl;O2;
(2)反应①是氯与氢氧化钙反应,是氯气的自身氧化还原,反应②是复分解反应,反应③是碳酸钙与盐酸反应也是复分解反应,反应④是二氧化碳、水、次氯酸钙反应生成次氯酸,是复分解反应,反应⑤是次氯酸分解,是氧化还反应,所以属于氧化还原反应的有①⑤,
故答案为:①⑤;
(3)反应①的化学方程式(并用双线桥法注明电子得失情况)为:
 ,
,故答案为:
 ;
;
点评:本题考查无机物的推断,题目综合考查元素化合物的性质以及应用,侧重于学生分析能力和综合运用化学知识的考查,突破口为B、A以及G的相关转化关系,题目难度中等.

练习册系列答案
相关题目
下列实验可实现鉴别目的是( )
| A、用BaCl2溶液鉴别SO3(g)和SO2 |
| B、用Ca(OH)2溶液鉴别Na2CO3溶液和NaHCO3溶液 |
| C、用CO2鉴别NaAlO2溶液和Na2SiO3溶液 |
| D、用湿润的碘化钾淀粉试纸鉴别Br2(g)和NO2 |
如图为水果电池的示意图,下列说法正确的是( )


| A、锌片作负极,质量逐渐减少 |
| B、电子由铜片沿导线流向锌片 |
| C、铜电极逐渐溶解 |
| D、该装置能将电能转化为化学能 |
有关物质用途的说法正确的是( )
| A、二氧化硅可用作半导体材料 |
| B、明矾可用于水的杀菌消毒 |
| C、碳酸氢钠可用于治疗胃酸过多 |
| D、硅可用于制造光导纤维 |
有关AgCl沉淀的溶解平衡说法正确的是( )
| A、AgCl沉淀生成和沉淀溶解不断进行,但速率相等 |
| B、AgCl难溶于水,溶液中没有Ag+和Cl- |
| C、在AgCl的澄清饱和溶液中,只要向其中加入NaCl溶液,一定会有沉淀生成 |
| D、向含有AgCl沉淀的悬浊液中加入NaCl固体,AgCl的溶解度增大 |
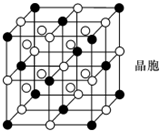 A,B,C,D,E,F都是短周期元素,原子序数依次增大,B,C同周期且相邻,A,D同主
A,B,C,D,E,F都是短周期元素,原子序数依次增大,B,C同周期且相邻,A,D同主 表示)位于该正方体的顶点和面心.该化合物的化学式是
表示)位于该正方体的顶点和面心.该化合物的化学式是