题目内容
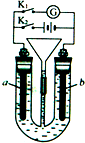 在如图所示装置中,U形管内装满稀H2SO4,a为铁电极,b为多孔石墨电极.
在如图所示装置中,U形管内装满稀H2SO4,a为铁电极,b为多孔石墨电极.(1)断开K2接通K1时,a为
(2)断开K1接通K2时,a为
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)断开K2接通K1时,形成原电池,活泼金属电极a是负极,b是正极,该极上发生得电子的还原反应2H++2e-=H2↑;
(2)断开K1接通K2时,a和电源的正极相连,是阳极,该极上金属本身失电子,电解硫酸的过程中,在阴极上氢离子得电子,所以氢离子浓度减小,酸性减弱,pH增大.
(2)断开K1接通K2时,a和电源的正极相连,是阳极,该极上金属本身失电子,电解硫酸的过程中,在阴极上氢离子得电子,所以氢离子浓度减小,酸性减弱,pH增大.
解答:
解:(1)断开K2接通K1时,形成原电池,活泼金属电极a是负极,b是正极,该极上发生得电子的还原反应2H++2e-=H2↑,故答案为:负;2H++2e-=H2↑;
(2)断开K1接通K2时,a和电源的正极相连,是阳极,该极上金属本身失电子,电极反应为Fe-2e-=Fe2+,电解硫酸的过程中,在阴极上氢离子得电子,所以氢离子浓度减小,酸性减弱,pH增大,故答案为:阳;Fe-2e-=Fe2+;增大.
(2)断开K1接通K2时,a和电源的正极相连,是阳极,该极上金属本身失电子,电极反应为Fe-2e-=Fe2+,电解硫酸的过程中,在阴极上氢离子得电子,所以氢离子浓度减小,酸性减弱,pH增大,故答案为:阳;Fe-2e-=Fe2+;增大.
点评:本题考查了电解池原理,明确离子放电顺序是解本题关键,结合电极反应进行解答,难度中等.

练习册系列答案
相关题目
下列实验装置能达到实验目的是( )
A、 除去Cl2中的HCl |
B、 从食盐水中提取氯化钠 |
C、 分离碘酒中的碘和酒精 |
D、 海水蒸馏得淡水 |
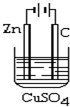
如图为水果电池的示意图,下列说法正确的是( )


| A、锌片作负极,质量逐渐减少 |
| B、电子由铜片沿导线流向锌片 |
| C、铜电极逐渐溶解 |
| D、该装置能将电能转化为化学能 |
在光照条件下,将a mol甲烷与足量Cl2反应,测知四种产物的物质的量比依次2:1:1:2,则耗Cl2的物质的量为( )
| A、a mol |
| B、1.25a mol |
| C、2.5a mol |
| D、4a mol |


 电解原理在工业有广泛的应用.利用相关知识回答下面的问题.
电解原理在工业有广泛的应用.利用相关知识回答下面的问题.