题目内容
14.下列说法不正确的是( )| A. | 苯甲酸共有四个同分异构体(含苯环且包括苯甲酸) | |
| B. | 相同条件下的沸点:乙二醇>乙醇>乙烷>甲烷 | |
| C. | CH3COOCH3在核磁共振氢谱中有两种不同类型的氢原子 | |
| D. | 两种不同的氨基酸在缩聚反应时可生成不少于4种的聚合物 |
分析 A.苯甲酸的同分异构体可以是酯,也可以是酚醛;
B.烷烃的相对分子质量越大,沸点越高;碳原子数越多,羟基数越多,沸点越高;相同碳原子的醇的沸点大于烷烃;
C.根据等效氢原子法判断分子中所含的不同氢原子的种类;
D.两种不同的氨基酸在缩聚反应时,可以是同种分子间,也可以是不同分子间,不同分子间至少有2种产物;
解答 解:A.苯甲酸的同分异构体可以甲酸苯酚酯,也可以是酚醛,羟基分别在醛基的邻位、间位、对位,有三种结构,苯甲酸共有五个同分异构体(含苯环且包括苯甲酸),故A错误;
B.烷烃的相对分子质量越大,沸点越高,则沸点:乙烷>甲烷;碳原子数越多,羟基数越多,沸点越高,则沸点:乙二醇>乙醇;相同碳原子的醇的沸点大于烷烃,所以沸点:乙二醇>乙醇>乙烷>甲烷,故B正确;
C.CH3COOCH3 有2种不同环境下的氢原子,故C正确;
D.两种不同的氨基酸在缩聚反应时,可以是同种分子间,有2种聚合物,也可以是不同分子间,不同分子间至少有2种产物,所以生成物不少于4种,故D正确;
故选A.
点评 本题主要考查了有机物结构与性质,难度不大,把握有机物的性质为解答的关键,注意规律性知识的应用.

练习册系列答案
相关题目
4.有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的:
为了鉴别上述化合物,分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴人到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,仅有B、C为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,只有A中放出无色气体,只有C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成.根据上述实验填空:
(1)写出B、C的化学式:BKNO3,CKAl(SO4)2.
(2)将含l mol A的溶液与含l mol E的溶液反应后蒸干,仅得到一种化合物,该化合物化学式为Na2CO3.
(3)C常用作净水剂,用离子方程式表示其净水原理Al3++3H2O?Al(OH)3+3H+.
(4)在A溶液中加入过量澄清石灰水,其离子方程式为2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+H2O.
(5)向20mL 2mol/L C溶液中加入60mL E溶液,充分反应后得到0.78g沉淀,则E溶液的物质的量浓度可能是0.5和2.5moI/L.
| 阳离子 | K+Na+Cu2+Al3+ |
| 阴离子 | SO42- HCO3-NO3-OH- |
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴人到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,仅有B、C为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,只有A中放出无色气体,只有C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成.根据上述实验填空:
(1)写出B、C的化学式:BKNO3,CKAl(SO4)2.
(2)将含l mol A的溶液与含l mol E的溶液反应后蒸干,仅得到一种化合物,该化合物化学式为Na2CO3.
(3)C常用作净水剂,用离子方程式表示其净水原理Al3++3H2O?Al(OH)3+3H+.
(4)在A溶液中加入过量澄清石灰水,其离子方程式为2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+H2O.
(5)向20mL 2mol/L C溶液中加入60mL E溶液,充分反应后得到0.78g沉淀,则E溶液的物质的量浓度可能是0.5和2.5moI/L.
6.7.2gXO中含有0.1mol氧原子,则X的相对原子质量为( )
| A. | 21.6 | B. | 28 | C. | 14 | D. | 56 |
17.取两支试管A、B,分别加入5mL 4%、5mL 12%的过氧化氢溶液,再各加入几滴0.2mol/L的氯化铁溶液.下列说法或操作正确的是( )
| A. | 、加入氯化铁的目的是加深溶液颜色,放大实验现象 | |
| B. | 、本实验的目的是研究浓度对双氧水分解速率的影响 | |
| C. | 、本实验过程中A、B试管都不明显,可以将那个很不明显的试管放入热水浴中来观察 | |
| D. | 、小明刚把A药品准备好,就有事情出去了,第二天继续这个实验来进行比较 |
18.下列有关说法正确的是( )
| A. | 将pH=10的浓氨水稀释,溶液中所有离子的浓度都减小 | |
| B. | CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H<0 | |
| C. | N2(g)+3H2(g)?2NH3(g)△H<0,其他条件不变时升高温度,反应速率V(H2)和氢气的平衡转化率均增大 | |
| D. | pH=3的盐酸和pH=11的氨水等体积混合液中,c(H+)<c(OH-) |
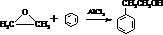 .
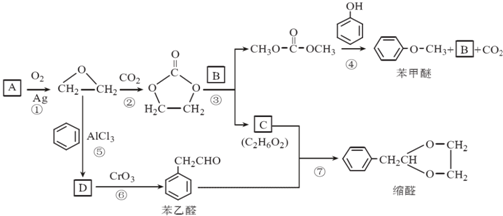
.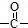 结构的苯乙醛的所有同分异构体的结构简式:
结构的苯乙醛的所有同分异构体的结构简式: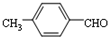 、
、 .
.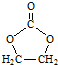 的合成路线,设计一条由2-氯丙烷和必要的无机试剂制备
的合成路线,设计一条由2-氯丙烷和必要的无机试剂制备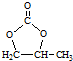 的合成路线(注明必要的反应条件)
的合成路线(注明必要的反应条件)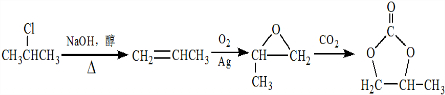 .
.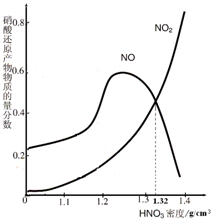 绿矾受热分解后的产物为不含硫元素的固体A、SO2、SO3和H2O.回答下列问题:
绿矾受热分解后的产物为不含硫元素的固体A、SO2、SO3和H2O.回答下列问题: