题目内容
19.4gH2中有2molH2,有4mol氢原子,有4NA个氢原子,有4NA个电子,有4mol质子.分析 结合n=$\frac{m}{M}$、N=nNA及分子构成计算.
解答 解:4gH2中有$\frac{4g}{2g/mol}$=2molH2,有2mol×2=4mol氢原子,有4mol×NA=4NA个氢原子,H的质子数=电子数=1,则有4NA个电子,有4mol质子,
故答案为:2;4;4NA;4NA;4.
点评 本题考查物质的量的计算,为高频考点,把握质量、物质的关系及分子构成为解答的关键,侧重分析与计算能力的考查,注意基本计算公式的应用,题目难度不大.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
10.下列各种说法正确的是( )
①铝用于软包装是利用了铝密度小的物理性质
②在加热条件下,FeO可以迅速变成Fe2O3
③合金材料可能含有非金属元素
④合成纤维和光导纤维都是新型无机非金属材料
⑤高纯度的硅广泛用于制作计算机芯片
⑥不能用自来水直接配制AgNO3溶液
⑦粗铜精炼时,纯铜与外电源的正极相连
⑧在金属元素和非金属元素的分界线附近可以寻找制备半导体材料的元素.
①铝用于软包装是利用了铝密度小的物理性质
②在加热条件下,FeO可以迅速变成Fe2O3
③合金材料可能含有非金属元素
④合成纤维和光导纤维都是新型无机非金属材料
⑤高纯度的硅广泛用于制作计算机芯片
⑥不能用自来水直接配制AgNO3溶液
⑦粗铜精炼时,纯铜与外电源的正极相连
⑧在金属元素和非金属元素的分界线附近可以寻找制备半导体材料的元素.
| A. | 仅②③④⑤⑥⑧ | B. | 仅③⑤⑥⑧ | C. | 仅①②④⑦ | D. | 除①外 |
7.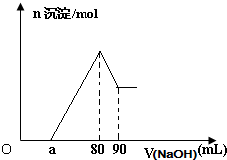 将一块镁铝合金投入一定体积的1mol/L稀盐酸中,待合金完全溶解后往溶液里滴入1mol/L的NaOH溶液,生成沉淀物质的量与加入NaOH溶液体积的关系如图.下列说法中不正确的是( )
将一块镁铝合金投入一定体积的1mol/L稀盐酸中,待合金完全溶解后往溶液里滴入1mol/L的NaOH溶液,生成沉淀物质的量与加入NaOH溶液体积的关系如图.下列说法中不正确的是( )
 将一块镁铝合金投入一定体积的1mol/L稀盐酸中,待合金完全溶解后往溶液里滴入1mol/L的NaOH溶液,生成沉淀物质的量与加入NaOH溶液体积的关系如图.下列说法中不正确的是( )
将一块镁铝合金投入一定体积的1mol/L稀盐酸中,待合金完全溶解后往溶液里滴入1mol/L的NaOH溶液,生成沉淀物质的量与加入NaOH溶液体积的关系如图.下列说法中不正确的是( )| A. | 由图可以确定该镁铝合金中铝的质量为0.27 g | |
| B. | 由图可以确定该合金中两元素的物质量之比的最大值为4 | |
| C. | 当滴入1mol/L的NaOH溶液85mL时,所得沉淀的成分为Mg(OH)2和Al(OH)3 | |
| D. | 由图可以确定a的取值范围为:0≤a≤50 |
14.下列说法不正确的是( )
| A. | 苯甲酸共有四个同分异构体(含苯环且包括苯甲酸) | |
| B. | 相同条件下的沸点:乙二醇>乙醇>乙烷>甲烷 | |
| C. | CH3COOCH3在核磁共振氢谱中有两种不同类型的氢原子 | |
| D. | 两种不同的氨基酸在缩聚反应时可生成不少于4种的聚合物 |
4.关于分散系的说法,正确的是( )
| A. | 根据体系的稳定性,可将分散系分为溶液、胶体和浊液 | |
| B. | 一种分散系的分散质可以是固态、液态或气态,但只能是纯净物 | |
| C. | 利用丁达尔效应可以区分溶液和胶体,它利用了光的衍射原理 | |
| D. | 火力发电厂的烟气管道里安装的静电除尘装置,它利用了胶体的电泳原理 |
2.下列离子方程式正确的是( )
| A. | 钠与水反应 Na+H2O═Na++OH-+H2↑ | |
| B. | 碳酸钠与稀硫酸反应CO32-+2H+═CO2↑+H2O | |
| C. | 氢氧化铜与稀硫酸反应OH-+H+═H2O | |
| D. | 铁与盐酸反应2Fe+6H+═2Fe3++3H2↑ |
 H++OH-、HCO3-+H2O
H++OH-、HCO3-+H2O +H2CO3+OH-、HCO3-+H2O
+H2CO3+OH-、HCO3-+H2O H3O++CO32-
H3O++CO32- 
 ,A的晶体类型离子晶体.
,A的晶体类型离子晶体.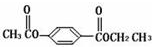
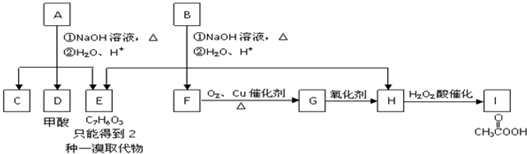
 $\stackrel{NaOH溶液,△}{→}$CH3COONa+
$\stackrel{NaOH溶液,△}{→}$CH3COONa+ -ONa)
-ONa)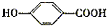 .
. 或
或 .
. ,反应类型是消去反应.
,反应类型是消去反应.