题目内容
9.在一定温度下,在恒压的密闭容器中进行的可逆反应A(g)+3B(g)?2C(g)达到平衡的标志是( )| A. | 混合气体密度保持不变 | |
| B. | 单位时间内生成n mol A,同时生成3n mol B | |
| C. | 混合气体的压强保持不变 | |
| D. | C生成的速率与A分解的速率相等 |
分析 可逆反应A(g)+3B(g)?2C(g)达到平衡状态时,正逆反应速率相等,各组分的浓度不再变化,据此进行解答.
解答 解:A.该反应为气体体积缩小的反应,恒压条件下容器的容积不断变化,当密度不变时,则容器的容积不再变化,说明达到平衡状态,故A正确;
B.单位时间内生成n mol A,同时生成3n mol B,表示的都是逆反应速率,无法判断正逆反应速率是否相等,故B错误;
C.由于在恒压条件下反应,则压强始终不变,不能根据压强变化判断平衡状态,故C错误;
D.C生成的速率与A分解的速率相等,由于A、C的计量数不相等,则正逆反应速率不相等,该反应没有达到平衡状态,故D错误;
故选A.
点评 本题考查了化学平衡状态的判断,题目难度中等,明确化学平衡及其影响因素为解答关键,注意该反应条件为恒压,为易错点,试题培养了学生的灵活应用能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
20.下列说法中正确的是( )
| A. | s区、d区、ds区都是金属元素 | |
| B. | p区都是主族元素 | |
| C. | 所有族中IIIB中元素种类最多 | |
| D. | 最外层电子数为2的元素都分布在s区 |
17.下列物质的转化在给定条件下能实现的是( )
| A. | NH3$→_{催化剂、加热}^{O_{2}}$NO2$\stackrel{H_{2}O}{→}$HNO3 | |
| B. | 海水$\stackrel{石灰乳}{→}$Mg(OH)2$\stackrel{HCi(aq)}{→}$MgCl2(aq)$\stackrel{△}{→}$ 无水MgCl2 | |
| C. | Al2O3$\stackrel{HCl(aq)}{→}$AlCl3(aq)$\stackrel{NH_{3}•H_{2}O}{→}$ 固体Al(OH)3 | |
| D. | CH2═CH2$→_{催化剂}^{H_{2}O}$CH3CH2OH$→_{△}^{CuO}$CH3COOH |
1.下列关于物质熔点的排列顺序,不正确的是( )
| A. | HI>HBr>HCl>HF | B. | CI4>CBr4>CCl4>CF4 | ||
| C. | NaCl>NaBr>KBr | D. | 金刚石>碳化硅>晶体硅 |
18.已知H2和O2反应放热,且破坏1mol H-H键、1mol O=O键,需吸收的能量分别为Q1 kJ、Q2kJ,形成1mol O-H键需释放Q3kJ.下列关系正确的是( )
| A. | Q1+Q2>Q3 | B. | Q1+Q2>2Q3 | C. | 2Q1+Q2<4Q3 | D. | 2Q1+Q2<2Q3 |
19.下列说法中不正确的是( )
| A. | 吸热反应不一定需要加热条件 | |
| B. | 放热反应只有化学键的形成,没有化学键的断开 | |
| C. | 化学反应除了生成新物质外,还伴随着能量的转化 | |
| D. | 稀酸和稀碱发生中和反应生成1 mol水所释放的热量称为中和热 |
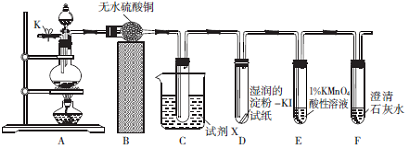
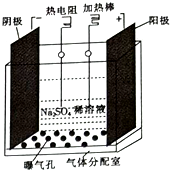 过氧化氢是实验室常用的试剂,在医疗、军事及工业上用途也非常广泛.回答下列问题:
过氧化氢是实验室常用的试剂,在医疗、军事及工业上用途也非常广泛.回答下列问题: