题目内容
19.下列说法中不正确的是( )| A. | 吸热反应不一定需要加热条件 | |
| B. | 放热反应只有化学键的形成,没有化学键的断开 | |
| C. | 化学反应除了生成新物质外,还伴随着能量的转化 | |
| D. | 稀酸和稀碱发生中和反应生成1 mol水所释放的热量称为中和热 |
分析 化学键角度:新化学键的形成所释放的能量小于破坏旧化学键所吸收的能量.
能量守恒角度:反应物的总能量小于生成物的总能量的化学反应,此过程与其反应条件无关,据此解答即可.
解答 解:A.氢氧化钡与氯化铵的反应在常温下就能进行,属于吸热反应,故A正确;
B.任何化学反应均有旧化学键的断裂和新化学键的生成,故B错误;
C.任何化学反应均伴随着能量的变化,故C正确;
D.稀的强酸和强碱发生反应恰好生成1mol水所放出的热量为中和热,故D错误,
故选BD.
点评 本题难度不大,考查化学中吸热或放热问题,熟记吸热或放热的判断规律是正确解答此类题的关键,对于特殊过程中的热量变化的要熟练记忆.

练习册系列答案
相关题目
9.在一定温度下,在恒压的密闭容器中进行的可逆反应A(g)+3B(g)?2C(g)达到平衡的标志是( )
| A. | 混合气体密度保持不变 | |
| B. | 单位时间内生成n mol A,同时生成3n mol B | |
| C. | 混合气体的压强保持不变 | |
| D. | C生成的速率与A分解的速率相等 |
7.把元素周期表中第16号元素和第6号元素的原子相比较,下列数据中前者是后者的4倍的是( )
| A. | 电子数 | B. | 最外层电子数 | C. | 中子数 | D. | 次外层电子数 |
8.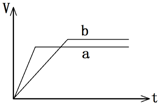 某同学在试管中用一定量的铁片与足量的稀硫酸反应,得到产生氢气的体积随时间变化的图象(b).若铁的用量不变,改变一个反应条件,得到图象(a).则改变的条件可能是( )
某同学在试管中用一定量的铁片与足量的稀硫酸反应,得到产生氢气的体积随时间变化的图象(b).若铁的用量不变,改变一个反应条件,得到图象(a).则改变的条件可能是( )
 某同学在试管中用一定量的铁片与足量的稀硫酸反应,得到产生氢气的体积随时间变化的图象(b).若铁的用量不变,改变一个反应条件,得到图象(a).则改变的条件可能是( )
某同学在试管中用一定量的铁片与足量的稀硫酸反应,得到产生氢气的体积随时间变化的图象(b).若铁的用量不变,改变一个反应条件,得到图象(a).则改变的条件可能是( )| A. | 向试管中滴加少许硫酸铜溶液 | B. | 在反应过程中对试管加热 | ||
| C. | 用铁粉代替铁片 | D. | 用98%的浓硫酸代替稀硫酸 |
9.X、Y、Z、W、R是短周期中的五种元素,其原子序数依次增大,X、W最外层电子数相等,X为地壳中含量最多的元素,Y是短周期中金属性最强的元素,Z单质是生活应用广泛的常见金属单质,下列说法不正确的是( )
| A. | 原子半径:Y>X | B. | 最高价氧化物的水化物的酸性:R>W | ||
| C. | 气态氢化物的稳定性:X>W | D. | 单质与水(或酸)反应的剧烈程度:Z>Y |
 .
. .
.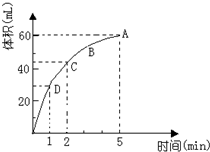 为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2粉末于 50mL密度为 1.1g/cm3的双氧水溶液中,通过实验测定:在标准状况下放
为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2粉末于 50mL密度为 1.1g/cm3的双氧水溶液中,通过实验测定:在标准状况下放