题目内容
16.(1)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视.它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势.氨的燃烧实验涉及下列两个相关的反应:①4NH3(g)+5O2(g)=4NO(g)+6H2O(l)△H1
②4NH3(g)+6NO(g)=5N2(g)+6H2O(l)△H2
则反应 4NH3(g)+3O2(g)=2N2(g)+6H2O(l)△H=$\frac{3△{H}_{1}+2△{H}_{2}}{5}$.(请用含有△H1、△H2的式子表示)
(2)若NH3?$\frac{1}{2}$N2+$\frac{3}{2}$H2 K=a,则N2+3H2?2NH3 K′=$\frac{1}{{a}^{2}}$.(用含a的式子表示)
(3)在体积为3L的恒容密闭容器中,合成氨N2+3H2?2NH3实验,投入4mol N2和9mol H2在一定条件下合成氨,平衡时仅改变温度测得的数据如表所示:
| 温度(K) | 平衡时NH3的物质的量(mol) |
| T1 | 2.4 |
| T2 | 2.0 |
①则T1<T2(填“>”、“<”或“=”)
②在T2下,经过10min达到化学平衡状态,则0~10min内H2的平均速率v(H2)=0.1mol•L-1•min-1,平衡时N2的转化率α(N2)=25%.
③下列图象分别代表焓变(△H)、混合气体平均相对分子质量($\overline{M}$)、N2体积分数φ(N2)和气体密度(ρ)与反应时间的关系,其中正确且能表明该可逆反应达到平衡状态的是BC.
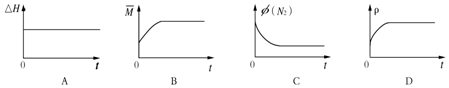
分析 (1)由①4NH3(g)+5O2(g)=4NO(g)+6H2O(l)△H1
②4NH3(g)+6NO(g)=5N2(g)+6H2O(l)△H2
结合盖斯定律可知,(①×3+②×2)×$\frac{1}{5}$得到4NH3(g)+3O2(g)=2N2(g)+6H2O(l);
(2)相同温度下,同一反应的正、逆反应的平衡常数互为倒数;同一转化关系,化学计量数变为原的n倍,则化学平衡常数为原来的n次方倍,以此来解答;
(3)破坏1mol N2(g)和3mol H2(g)中的化学键消耗的总能量小于破坏2mol NH3(g)中的化学键消耗的能量,则合成氨的反应为放热反应,
①由表格数据可知,T1对应的氨气平衡时物质的量大,则T1的温度低;
②T2K下,经过10min达到化学平衡状态,则
N2+3 H2?2NH3,
开始 4 9 0
转化 1 3 2
平衡 3 6 2
结合v=$\frac{△c}{△t}$及转化率计算;
③焓变(△H)始终不变,混合气体平均相对分子质量为变量、N2体积分数φ(N2)为变量,气体密度(ρ)始终不变.
解答 解:(1)由①4NH3(g)+5O2(g)=4NO(g)+6H2O(l)△H1
②4NH3(g)+6NO(g)=5N2(g)+6H2O(l)△H2
结合盖斯定律可知,(①×3+②×2)×$\frac{1}{5}$得到4NH3(g)+3O2(g)=2N2(g)+6H2O(l),则△H=$\frac{3△{H}_{1}+2△{H}_{2}}{5}$,
故答案为:$\frac{3△{H}_{1}+2△{H}_{2}}{5}$;
(2)若NH3?$\frac{1}{2}$N2+$\frac{3}{2}$H2 K=a,则N2+3H2?2NH3 K′=$\frac{1}{{a}^{2}}$,
故答案为:$\frac{1}{{a}^{2}}$;
(3)破坏1mol N2(g)和3mol H2(g)中的化学键消耗的总能量小于破坏2mol NH3(g)中的化学键消耗的能量,则合成氨的反应为放热反应,
①由表格数据可知,T1对应的氨气平衡时物质的量大,则T1的温度低,则T1<T2,
故答案为:<;
②T2K下,经过10min达到化学平衡状态,则
N2+3 H2?2NH3,
开始 4 9 0
转化 1 3 2
平衡 3 6 2
v(H2)=$\frac{△c}{△t}$=$\frac{\frac{3mol}{3L}}{10min}$=0.1mol•L-1•min-1,
平衡时N2的转化率α(N2)=$\frac{1}{4}$×100%=25%,
故答案为:0.1mol•L-1•min-1;25%;
③焓变(△H)始终不变,混合气体平均相对分子质量($\overline{M}$)为变量、N2体积分数φ(N2)为变量,气体密度(ρ)始终不变,随反应进行,气体的物质的量减小,则 $\overline{M}$随时间增大而增大,直到达到平衡状态不变;N2体积分数逐渐减小,到达到平衡状态不变,由图可知,正确且能表明该可逆反应达到平衡状态的为BC,
故答案为:BC.
点评 本题考查了盖斯定律的应用、化学平衡常数及计算,把握化学平衡常数的意义、化学反应的关系为解答的关键,侧重分析与计算能力的考查,注意反应中化学计量数的关系,题目难度中等.

 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案 已知A(g)+B(g)?C(g)+D(s)反应的平衡常数与温度的关系如下:
已知A(g)+B(g)?C(g)+D(s)反应的平衡常数与温度的关系如下:| 温度℃ | 700 | 800 | 880 | 1000 | 1200 |
| 平衡常数 | 1.0 | 10.0 | 12.5 | 16.1 | 17.7 |
(1)该反应的平衡常数表达式K=$\frac{c(C)}{c(A)c(B)}$,△H>0(填“>、<、或=”);
(2)800℃时,向一个5L的密闭容器中充入0.4molA和0.7molB,若反应初始2mim内A的平均反应速率为0.01mol•L-1•min-1,则2min时c(A)=0.06mol•L-1,C的物质的量为0.1mol;若经过一段时间后,反应达到平衡时再向容器中充入0.4molA,则再次达到平衡后A的百分含量与第一次平衡相比增大(填“增大”、“减小”、或“不变”)
(3)下列选项中能作为判断反应达到平衡的依据有ad
a.压强不随时间改变
b.v(A):v(b)=1:1
c.单位时间内消耗A和B的物质的量相等
d.C的百分含量保持不变
(4)880℃时,反应 C(g)+D(s)?A(g)+B(g)的平衡常数的值为0.08.
(5)某温度时,平衡浓度符合下式:c(A).c(B)=c(C),则该此时的温度为700℃.
(6)图是1000℃时容器中A的物质的量的变化曲线,请在图中补画出该反应在1200℃时A的物质的量的变化曲线图
 .
. | A. | 石灰水与盐酸的反应 OH-+H+═H2O | |
| B. | 氧化铜与盐酸反应 O2-+2H+═H2O | |
| C. | 铜片插入硝酸银溶液中 Cu+Ag+═Cu2++Ag | |
| D. | 碳酸钙溶于醋酸中 CaCO3+2H+═Ca2++H2O+CO2↑ |
| A. | 溶液中导电粒子的数目减小 | |
| B. | 溶液中$\frac{c(C{H}_{3}CO{O}^{-})•c({H}^{+})}{c(C{H}_{3}COOH)}$不变 | |
| C. | 醋酸的电离程度增大,c(H+)亦增大 | |
| D. | 醋酸的电离常数K随醋酸浓度减小而减小 |
| A. | NaCl晶体 | B. | 液态氯化氢 | C. | 熔融的KNO3 | D. | NH3•H2O |
①同质量、不同密度的Cl2和CO ②同温度、同体积的H2和 N2
③同体积、同密度的 C2H4和C3H6两种气体 ④同压强、同体积的N2O 和 CO2两种气体.
| A. | ①③ | B. | ③ | C. | ③④ | D. | ②④ |
| A. | 配制一定物质的量浓度的溶液实验中,定容时,俯视观察刻度线,会引起配制溶液的浓度偏高 | |
| B. | 分液漏斗中上层和下层液体均可以从下口流出 | |
| C. | 冷凝管使用时冷水既可以从上口进也可以从下口进 | |
| D. | 不能用丁达尔效应鉴别Fe(OH)3胶体和CuSO4溶液 |
| A. | Na | B. | FeCl3溶液 | C. | KMnO4酸性溶液 | D. | 溴水 |
 .
.