题目内容
5.科学的实验方法为我们探索物质世界提供了一把金钥匙.下列实验方法正确的是( )| A. | 配制一定物质的量浓度的溶液实验中,定容时,俯视观察刻度线,会引起配制溶液的浓度偏高 | |
| B. | 分液漏斗中上层和下层液体均可以从下口流出 | |
| C. | 冷凝管使用时冷水既可以从上口进也可以从下口进 | |
| D. | 不能用丁达尔效应鉴别Fe(OH)3胶体和CuSO4溶液 |
分析 A.配制一定物质的量浓度溶液时,定容时俯视刻度线导致配制溶液体积偏小;
B.分液时,上层液体从上口倒出,下层液体从下口倒出;
C.冷凝管中的水采用逆流方式;
D.胶体具有丁达尔效应,溶液没有丁达尔效应.
解答 解:A.配制一定物质的量浓度溶液时,定容时俯视刻度线导致配制溶液体积偏小,溶质的物质的量不变,导致配制溶液浓度偏高,故A正确;
B.分液时,上层液体从上口倒出,下层液体从下口倒出,否则引进杂质,故B错误;
C.冷凝管中的水采用逆流方式,所以冷凝管使用时冷水既从下口进也可以从上口进,否则馏分急剧冷却而炸裂冷凝管,故C错误;
D.胶体具有丁达尔效应,溶液没有丁达尔效应,所以可以用丁达尔效应鉴别Fe(OH)3胶体和CuSO4溶液,故D错误;
故选A.
点评 本题考查化学实验方案评价,为高频考点,涉及溶液配制、分液、馏分冷凝、物质鉴别等知识点,侧重考查实验操作、实验评价能力,明确实验原理及实验操作规范性是解本题关键,易错点是A中误差分析,题目难度不大.

练习册系列答案
相关题目
16.(1)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视.它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势.氨的燃烧实验涉及下列两个相关的反应:
①4NH3(g)+5O2(g)=4NO(g)+6H2O(l)△H1
②4NH3(g)+6NO(g)=5N2(g)+6H2O(l)△H2
则反应 4NH3(g)+3O2(g)=2N2(g)+6H2O(l)△H=$\frac{3△{H}_{1}+2△{H}_{2}}{5}$.(请用含有△H1、△H2的式子表示)
(2)若NH3?$\frac{1}{2}$N2+$\frac{3}{2}$H2 K=a,则N2+3H2?2NH3 K′=$\frac{1}{{a}^{2}}$.(用含a的式子表示)
(3)在体积为3L的恒容密闭容器中,合成氨N2+3H2?2NH3实验,投入4mol N2和9mol H2在一定条件下合成氨,平衡时仅改变温度测得的数据如表所示:
已知:破坏1mol N2(g)和3mol H2(g)中的化学键消耗的总能量小于破坏2mol NH3(g)中的化学键消耗的能量.
①则T1<T2(填“>”、“<”或“=”)
②在T2下,经过10min达到化学平衡状态,则0~10min内H2的平均速率v(H2)=0.1mol•L-1•min-1,平衡时N2的转化率α(N2)=25%.
③下列图象分别代表焓变(△H)、混合气体平均相对分子质量($\overline{M}$)、N2体积分数φ(N2)和气体密度(ρ)与反应时间的关系,其中正确且能表明该可逆反应达到平衡状态的是BC.
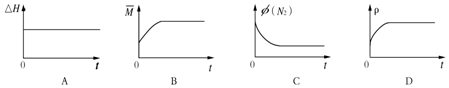
①4NH3(g)+5O2(g)=4NO(g)+6H2O(l)△H1
②4NH3(g)+6NO(g)=5N2(g)+6H2O(l)△H2
则反应 4NH3(g)+3O2(g)=2N2(g)+6H2O(l)△H=$\frac{3△{H}_{1}+2△{H}_{2}}{5}$.(请用含有△H1、△H2的式子表示)
(2)若NH3?$\frac{1}{2}$N2+$\frac{3}{2}$H2 K=a,则N2+3H2?2NH3 K′=$\frac{1}{{a}^{2}}$.(用含a的式子表示)
(3)在体积为3L的恒容密闭容器中,合成氨N2+3H2?2NH3实验,投入4mol N2和9mol H2在一定条件下合成氨,平衡时仅改变温度测得的数据如表所示:
| 温度(K) | 平衡时NH3的物质的量(mol) |
| T1 | 2.4 |
| T2 | 2.0 |
①则T1<T2(填“>”、“<”或“=”)
②在T2下,经过10min达到化学平衡状态,则0~10min内H2的平均速率v(H2)=0.1mol•L-1•min-1,平衡时N2的转化率α(N2)=25%.
③下列图象分别代表焓变(△H)、混合气体平均相对分子质量($\overline{M}$)、N2体积分数φ(N2)和气体密度(ρ)与反应时间的关系,其中正确且能表明该可逆反应达到平衡状态的是BC.
13.氯化铁溶液与氢氧化铁胶体具有的共同性质是( )
| A. | 都能产生丁达尔效应 | |
| B. | 有相同的颜色 | |
| C. | 分散质颗粒直径都在1-100nm之间 | |
| D. | 加入浓氢氧化钠溶液都产生红褐色沉淀 |
20.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 常温常压下,22.4 L CCl4、CO2含有的分子数为NA | |
| B. | 通常状况下,NA个CO2分子占有的体积约为22.4 L | |
| C. | 常温常压下,1.06 g Na2CO3含有的Na+离子数为0.02NA | |
| D. | 物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为NA |
15.对于工业合成氨反应:N2+3H2?2NH3,下列说法错误的是( )
| A. | 使用合适的催化剂可以加大反应速率 | |
| B. | 升高温度可以增大反应速率 | |
| C. | 增大N2浓度可以使H2转化率达到100% | |
| D. | 增大N2浓度可以减小反应速率 |

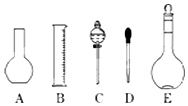 实验室需要0.1mol/L NaOH溶液500mL.根据这种溶液的配制情况回答下列问题:
实验室需要0.1mol/L NaOH溶液500mL.根据这种溶液的配制情况回答下列问题: