题目内容
13.SiCl4的分子结构与CCl4类似,对其作出如下推断:①SiCl4是正四面体构型:②常温常压下SiCl4是液体;③SiCl4的分子是由极性键形成的分子;④SiCl4熔点高于CCl4.其中正确的是( )| A. | 只有① | B. | 只有①② | C. | 只有②③ | D. | ①②③④ |
分析 SiCl4的分子结构与CCl4类似,与CCl4根据的结构和性质分析,CCl4属于分子晶体,常温为液体,含有共价键,分子晶体的相对分子质量越大,沸点越高,据此分析.
解答 解:SiCl4的分子结构与CCl4类似,与CCl4根据的结构和性质分析,CCl4属于分子晶体,常温为液体,含有共价键,分子晶体的相对分子质量越大,熔点越高,
①CCl4结构价层电子对数为4,没有孤对电子对,故空间结构为正四面体结构,SiCl4与CCl4结构相似,也为正四面体,故正确;
②SiCl4与CCl4结构相似,常温常压下SiCl4是液体,故正确;
③SiCl4中Si与Cl形成共价键,则SiCl4是由极性共价键形成的分子,故正确;
④分子晶体的相对分子质量越大,熔点越高,则SiCl4熔点高于CCl4,故正确;
所以正确的有①②③④;
故选D.
点评 本题考查了物质的结构和性质,采用类比法分析,题目难度不大,注意把握CCl4的结构和性质.

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
8.一定条件下,将3molA和1molB两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)?xC(g)+2D(s).2min末该反应达到平衡,生成0.8molD,并测得C的浓度为0.4mol/L.下列判断正确的是( )
| A. | x=1 | |
| B. | A的平均反应速率为0.3mol/(L•s) | |
| C. | B的转化率为60% | |
| D. | 若混合气体的密度不再改变时,该反应一定达到平衡状态 |
18.把1L含乙烯和H2的混合气体通过Ni催化剂,使乙烯和H2发生加成反应,完全反应后,气体体积变为yL(气体体积均在同温、同压下测定).若乙烯在1L混合气体中的体积分数为a%,则a%和y的关系一定不正确的是( )
| A. | y=1×a% | B. | y=1-1×a% | C. | y=1×a%=0.5 | D. | y=1-1×a%<0.5 |
5.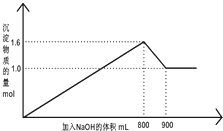 向1L A1Cl3和FeCl3的混合溶液,逐滴加入NaOH 的溶液.产生沉淀的物质的量和加入溶液的体积的关系如图所示,回答下列问题:
向1L A1Cl3和FeCl3的混合溶液,逐滴加入NaOH 的溶液.产生沉淀的物质的量和加入溶液的体积的关系如图所示,回答下列问题:
(1)加入NaOH 溶液900mL 时,溶液中的沉淀是Fe(OH)3,溶液中的溶质是NaCl、NaAlO2.(填化学式)
(2)加入NaOH 溶液800mL 至900mL 之间时,发生的离子反应方程式是Al(OH)3+OH-=AlO2-+2H2O
(3)将混合溶液中各溶质的物质的量浓度填入下表:
(4)加入NaOH 的溶液物质的量浓度为8mol/L.
 向1L A1Cl3和FeCl3的混合溶液,逐滴加入NaOH 的溶液.产生沉淀的物质的量和加入溶液的体积的关系如图所示,回答下列问题:
向1L A1Cl3和FeCl3的混合溶液,逐滴加入NaOH 的溶液.产生沉淀的物质的量和加入溶液的体积的关系如图所示,回答下列问题:(1)加入NaOH 溶液900mL 时,溶液中的沉淀是Fe(OH)3,溶液中的溶质是NaCl、NaAlO2.(填化学式)
(2)加入NaOH 溶液800mL 至900mL 之间时,发生的离子反应方程式是Al(OH)3+OH-=AlO2-+2H2O
(3)将混合溶液中各溶质的物质的量浓度填入下表:
| 溶质 | A1Cl3 | FeCl3 |
| 物质的量浓度 mol/L |
2.下列有关共价化合物的说法中,一定正确的是( )
①具有较低的熔、沸点
②不是电解质
③固体时是分子晶体
④都由分子构成
⑤液态时不导电.
①具有较低的熔、沸点
②不是电解质
③固体时是分子晶体
④都由分子构成
⑤液态时不导电.
| A. | ①③④ | B. | ②④⑤ | C. | ①②③④⑤ | D. | 只有⑤ |

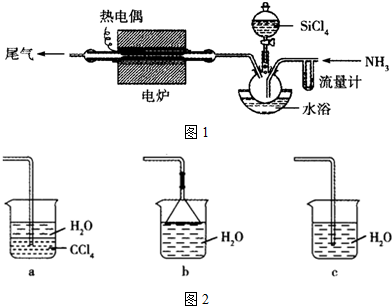
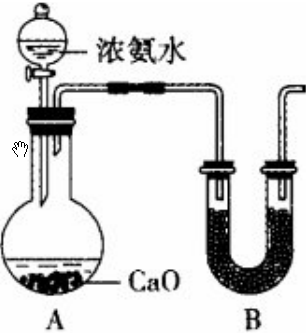
 甲、乙、丙、丁、戊为原子序数依次增大的短周期元素.甲、丙处于同一主族,丙、丁、戊处于同一周期,戊原子的最外层电子数是甲、乙、丙原子最外层电子数之和.甲、乙组成的常见气体X能使湿润的红色石蕊试纸变蓝;戊的单质与X反应能生成乙的单质,同时生成两种溶于水均呈酸性的化合物Y和Z,0.1 mol/L的Y溶液pH>1;丁的单质既能与丙元素最高价氧化物的水化物的溶液反应生成盐L,也能与Z的水溶液反应生成盐;丙、戊可组成化合物M.
甲、乙、丙、丁、戊为原子序数依次增大的短周期元素.甲、丙处于同一主族,丙、丁、戊处于同一周期,戊原子的最外层电子数是甲、乙、丙原子最外层电子数之和.甲、乙组成的常见气体X能使湿润的红色石蕊试纸变蓝;戊的单质与X反应能生成乙的单质,同时生成两种溶于水均呈酸性的化合物Y和Z,0.1 mol/L的Y溶液pH>1;丁的单质既能与丙元素最高价氧化物的水化物的溶液反应生成盐L,也能与Z的水溶液反应生成盐;丙、戊可组成化合物M.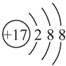 .
.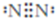 .
.