题目内容
13.元素X、Y、Z、W的原子序数依次增大,且原子序数之和为22,最外层电子数之和为16,在化合物Y2X2、Z2X4、X2W2中,相应分子内各原子最外层电子都满足相应稳定结构.下列说法正确的是( )| A. | X、Y、Z、W的原子半径的大小关系为:W>Y>Z>X | |
| B. | 在化合物Y2X2、Z2X4、X2W2中,分子所含的共用电子对数相等 | |
| C. | 与元素Y、Z相比,元素W形成的简单氢化物最稳定,是因为其分子间存在氢键 | |
| D. | X、Y、Z、W四种元素可形成化学式为Y2X5ZW2的化合物 |
分析 元素X、Y、Z、W的原子序数依次增大,且原子序数之和为22,最外层电子数之和为16,均为短周期元素,在化合物Y2X2、Z2X4、X2W2中,相应分子内各原子最外层电子都满足稳定结构,则X应为H,Y为C,Z为N,W为O,形成的化合物分别为C2H2、N2H4、H2O2,以此解答该题.
解答 解:元素X、Y、Z、W的原子序数依次增大,且原子序数之和为22,最外层电子数之和为16,均为短周期元素,在化合物Y2X2、Z2X4、X2W2中,相应分子内各原子最外层电子都满足稳定结构,则X应为H,Y为C,Z为N,W为O,形成的化合物分别为C2H2、N2H4、H2O2.
A.X、Y、Z、W的原子半径的大小关系为Y(C)>Z(N)>W(O)>X(H),故A错误;
B.在化合物C2H2、N2H4、H2O2中,含有的电子对数分别为5、5、3,不相等,故B错误;
C.氢化物的稳定性与氢键无关,与共价键的强弱有关,故C错误;
D.X、Y、Z、W四种元素可形成化学式为H7C2NO2的化合物,为CH2OH-CH(OH)NH2,故D正确.
故选D.
点评 本题考查元素化合物推断、原子结构与元素周期律的关系,明确元素的种类为解答该题的关键,属于猜测验证型推断,题目难度中等.

练习册系列答案
相关题目
3.将红磷和硫分别在如图所示的两个盛满O2的集气瓶内燃烧,待燃烧完毕后,同时打开两个止水夹,这时观察到的现象是( )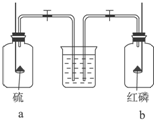

| A. | 水先进入a瓶 | B. | 水先进入b瓶 | ||
| C. | 水同时进入两瓶 | D. | 水不进入任何一瓶 |
4.下列反应 不属于取代反应的是( )
| A. | CH4+Cl2$\stackrel{光}{→}$CH3Cl+HCl | |
| B. | CH2═CH2+HBr-→CH3-CH2Br | |
| C. | CH3CH2OH+CH3COOH$→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O | |
| D. | 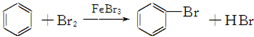 |
8.X元素原子的最外层电子数与次外层电子数的差值等于电子层数;Y元素原子比X元素原子的最外层电子数多2.则X与Y所形成的化合物为( )
| A. | X3Y2 | B. | X2Y | C. | XY2 | D. | XY3 |
18.下列叙述中正确的是( )
| A. | 若烃中碳、氢元素的质量分数相同,则为同系物 | |
| B. | CH2═CH2和CH2═CH-CH═CH2互为同系物 | |
| C. | 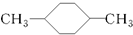 和 和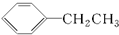 互为同分异构体 互为同分异构体 | |
| D. | 同分异构体的化学性质可能相似 |
5.下列说法正确的是( )
| A. | 需要加热才能发生的反应是吸热反应 | |
| B. | 反应放出的热量的多少与反应物的质量和状态无关 | |
| C. | 若氢气和氧气化合是放热反应,则电解水生成氢气和氧气是吸热反应 | |
| D. | 对放热反应A+B→C+D,A、B的能量总和小于C、D的能量总和 |
2.某化合物6.4g在氧气中完全燃烧,只生成8.8gCO2和5.4gH2O.下列说法正确的是( )
| A. | 该化合物仅含碳、氢两种元素 | B. | 该化合物中碳、氢原子个数比为1:2 | ||
| C. | 该有机物的分子式为C2H6 | D. | 该化合物中一定含有氧元素 |
3.已知下列反应的热化学方程式为
(1)CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H1=-870.3kJ•mol-1
(2)C(s)+O2(g)═CO2(g)△H2=-393.5kJ•mol-1
(3)H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H3=-285.8kJ•mol-1
则反应2C(s)+2H2(g)+O2(g)═CH3COOH(l)的△H为( )
(1)CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H1=-870.3kJ•mol-1
(2)C(s)+O2(g)═CO2(g)△H2=-393.5kJ•mol-1
(3)H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H3=-285.8kJ•mol-1
则反应2C(s)+2H2(g)+O2(g)═CH3COOH(l)的△H为( )
| A. | -488.3 kJ•mol-1 | B. | -191 kJ•mol-1 | ||
| C. | -476.8 kJ•mol-1 | D. | -1 549.6 kJ•mol-1 |