题目内容
7.用如图装置测定水中氢、氧元素的质量比,方法是分别测定通氢气前后玻璃管的质量差和U型管的质量差,实验测得m(H):m(O)>1:8.下列对导致这一结果的原因的分析中,不正确的是( )
| A. | Ⅰ、Ⅱ装置之间缺少干燥装置 | B. | Ⅱ装置中玻璃管内有水冷凝 | ||
| C. | Ⅱ装置中CuO没有全部被还原 | D. | Ⅲ装置后缺少干燥装置 |
分析 由图可知,I中Zn与稀硫酸反应生成氢气,I与Ⅱ装置之间缺少干燥装置,干燥氢气后,Ⅱ中氢气与CuO发生氧化还原反应,Ⅲ中吸收水,Ⅲ装置后缺少干燥装置,分别测定通氢气前后玻璃管的质量差和U型管的质量差,Ⅱ中质量差为O元素的质量,Ⅲ中质量差为水的质量,以此来解答.
解答 解:Ⅱ中质量差为O元素的质量,Ⅲ中质量差为水的质量,
A.Ⅰ、Ⅱ装置之间缺少干燥装置,测定水的质量偏大,则m(H):m(O)>1:8,故A正确;
B.Ⅱ装置中玻璃管内有水冷凝,Ⅱ中质量差为O元素的质量偏小,则m(H):m(O)>1:8,故B正确;
C.Ⅱ中质量差为O元素的质量,与CuO没有全部被还原无关,故C错误;
D.Ⅲ装置后缺少干燥装置,可吸收空气中的水,则测定水的质量偏大,则m(H):m(O)>1:8,故D正确;
故选C.
点评 本题考查物质组成及含量测定实验,为高频考点,把握实验装置的作用、实验技能为解答的关键,侧重分析与实验能力的考查,注意物质组成的测定方法,题目难度不大.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
17.下列有关非金属及其化合物的说法正确的是( )
| A. | 硅酸可使紫色石蕊试液变红色 | |
| B. | 二氧化硫通入紫色石蕊试液中.试液先变红后褪色 | |
| C. | 可用锌粒与稀硝酸反应制备氢气 | |
| D. | 液溴易挥发,所以存放液溴的试剂瓶中应加水封保存 |
2.下列说法不正确的是( )
| A. | 蛋白质水解的最终产物是氨基酸 | |
| B. | 油脂水解生成甘油和高级脂肪酸或高级脂肪酸盐 | |
| C. | 淀粉水解的最终产物是葡萄糖 | |
| D. | 重油裂解可以得到汽油 |
19.有常温下物质的量浓度均为0.1mo/L的①氨水②NH4Cl溶液③Na2CO3溶液④NaHCO3溶液,下列说法正确的是( )
| A. | 4种溶液pH的大小顺序:①>④>③>② | |
| B. | 等体积的①和②溶液混合后pH>7,c(NH3•H2O)>c( NH4+) | |
| C. | 溶液①、③由水电离产生的c(OH-):①<③ | |
| D. | 溶液③、④等体积混合后,溶液中c(CO32-)>c(HCO3-) |
16.为了除去硫酸铜溶液中含有的Fe2+杂质,先加入合适的氧化剂使Fe2+氧化为Fe3+,然后再调节溶液的pH值,下列物质中最好选用( )
| A. | Cl2水,NaOH(aq) | B. | KMnO4(aq),氨水 | C. | H2O2溶液,氧化铜 | D. | HNO3(aq),氨水 |



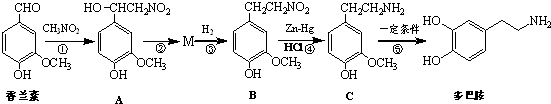
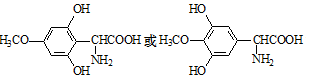 .
.