题目内容
3.过量的Fe与一定量的稀硫酸反应制取氢气,一定温度下为加快反应速率而又不影响氢气的量,可向其中加入少量的( )| A. | CuSO4晶体 | B. | Cu(NO3)2晶体 | C. | CH3COOK固体 | D. | SO3固体 |
分析 适当增大稀硫酸浓度、升高温度、增大反应物接触面积、形成原电池等都能加快反应速率,但不影响生成氢气的量,则改变条件时不能降低氢离子总物质的量,据此分析解答.
解答 解:A.Fe能置换出Cu,Fe、Cu和稀硫酸构成原电池而加快反应速率,但不影响硫酸电离出氢离子总物质的量,所以能加快反应速率但不影响氢气的量,故A正确;
B.加入硝酸铜后相当于含有硝酸,Fe和稀硝酸反应生成NO而不是氢气,所以降低氢气的量,故B错误;
C.加入醋酸钾后生成醋酸,醋酸是弱电解质导致溶液中氢离子浓度降低,反应速率降低,但不影响生成氢气的量,故C错误;
D.加入三氧化硫固体,三氧化硫和水反应生成硫酸而增大氢离子浓度,反应速率加快,但生成氢气质量增大,故D错误;
故选A.
点评 本题考查化学反应速率影响因素,为高频考点,明确化学反应速率影响原理是解本题关键,易错选项是B,注意隐含条件的挖掘,题目难度不大.

练习册系列答案
相关题目
18.下列判断正确的是( )
| A. | Ca(OH)2微溶于水,所以Ca(OH)2是弱电解质 | |
| B. | 强电解质溶液的导电能力可能比弱电解质溶液导电能力弱 | |
| C. | Cu、NaCl溶液不是电解质,所以是非电解质 | |
| D. | SO3溶于水后导电,所以SO3是电解质 |
15.某同学组装了如图所示的电化学装置,电极Ⅰ为Al,其他电极均为Cu,则下列叙述中正确的是( )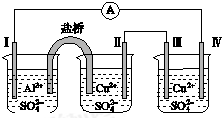

| A. | 电极Ⅰ发生还原反应 | B. | 电流方向:电极Ⅳ→ →电极Ⅰ →电极Ⅰ | ||
| C. | 电极Ⅱ逐渐溶解 | D. | 电极Ⅲ的电极反应:Cu2++2e-═Cu |
12.把下列各组物质同时加入水中,只得到无色透明溶液的是( )
| A. | K2SO4 HCl BaCl2 | B. | Na2CO3 K2SO4 KCl | ||
| C. | FeCl3 NaCl KOH | D. | CuSO4 HCl NaNO3 |
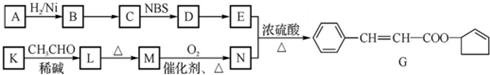
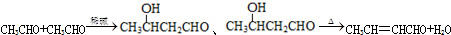
 ,D中官能团的名称为碳碳双键、溴原子.
,D中官能团的名称为碳碳双键、溴原子. .
.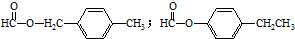 .
.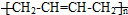 )的合成路线:CH3CH2CH2CH2OH$→_{△}^{浓硫酸}$CH3CH2CH=CH2$\stackrel{NBS}{→}$CH3CHBrCH=CH2$→_{△}^{NaOH醇溶液}$CH2=CHCH=CH2
)的合成路线:CH3CH2CH2CH2OH$→_{△}^{浓硫酸}$CH3CH2CH=CH2$\stackrel{NBS}{→}$CH3CHBrCH=CH2$→_{△}^{NaOH醇溶液}$CH2=CHCH=CH2 .
.
 醋酸是日常生活中常见的弱酸.
醋酸是日常生活中常见的弱酸.