题目内容
2.设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )| A. | 25℃时,1L pH=13的Ba(OH)2溶液中含有OH一的数目为0.2NA | |
| B. | 取50mL 14.0moI/L浓硝酸与足量的铜片反应,生成气体分子的数目为0.35NA | |
| C. | 标准状况下,2.24L二氧化硫中含有的电子总数为3.2NA | |
| D. | 40g金刚砂(SiC)中含有C-Si键的个数为2NA |
分析 A、pH=13的氢氧化钡溶液中,氢氧根的浓度为0.1mol/L;
B、取50mL 14.0moI/L浓硝酸与足量的铜片反应,开始生成的是NO2,随着硝酸变稀,生成的气体为NO、N2等;
C、求出二氧化硫的物质的量,然后根据1mol二氧化硫中含32mol电子来分析;
D、求出金刚砂的物质的量,然后根据1mol金刚砂中含4molSi-C键来分析.
解答 解:A、pH=13的氢氧化钡溶液中,氢氧根的浓度为0.1mol/L,故1L溶液中含有的氢氧根的物质的量为0.1mol,则个数为0.1NA个,故A错误;
B、取50mL 14.0moI/L浓硝酸与足量的铜片反应,开始生成的是NO2,随着硝酸变稀,生成的气体为NO、N2等,故生成的气体分子个数小于0.35NA个,故B错误;
C、标况下2.24L二氧化硫的物质的量为0.1mol,而1mol二氧化硫中含32mol电子,故0.1mol二氧化硫中含3.2NA个电子,故C正确;
D、40g金刚砂的物质的量为1mol,而1mol金刚砂中含4molSi-C键,即含4NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
12.下列过程中属于人工固氮的是( )
| A. | 雷雨天气时产生少量NO | |
| B. | 往农田中施放铵态氮肥 | |
| C. | 豆科植物等根部的根瘤菌吸收空气中的氮气转变为氨 | |
| D. | N2和H2在高温、高压和催化剂存在下合成氨 |
13.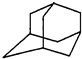 如图是金刚烷的结构示意图,1-溴金刚烷可用于合成甲型流感病毒的抑制剂.下列有关说法中正确的是( )
如图是金刚烷的结构示意图,1-溴金刚烷可用于合成甲型流感病毒的抑制剂.下列有关说法中正确的是( )
 如图是金刚烷的结构示意图,1-溴金刚烷可用于合成甲型流感病毒的抑制剂.下列有关说法中正确的是( )
如图是金刚烷的结构示意图,1-溴金刚烷可用于合成甲型流感病毒的抑制剂.下列有关说法中正确的是( )| A. | 金刚烷的分子中有18个碳原子 | |
| B. | 1-溴金刚烷的结构有2种 | |
| C. | 金刚烷属于烷烃的同系物 | |
| D. | 金刚烷应该具有和芳香烃相似的化学性质 |
7.用右图所示装置模拟电解原理在工业生产上的应用.下列说法正确的是( )
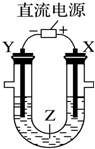

| A. | 氯碱工业中,X电极上反应式是4OH--4e-═2H2O+O2↑ | |
| B. | 电解精炼铜时,Z溶液中的铜离子浓度不变 | |
| C. | 在铁片上镀铜时,Y是纯铜 | |
| D. | 电解水制氢气时,Z可以是稀硫酸溶液 |
11.下列反应是氧化还原反应的是( )
| A. | NaOH+HCl═NaCl+H2O | B. | CuO+H2SO4═CuSO4+H2O | ||
| C. | Zn+2H+═Zn2++H2↑ | D. | CaO+H2O═Ca(OH)2 |
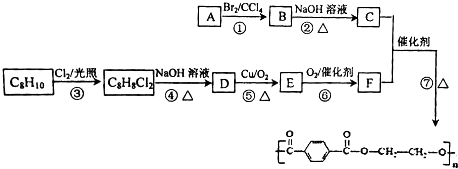
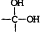 →
→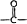 +H2O
+H2O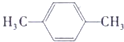 .
.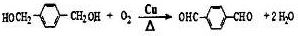 ;
;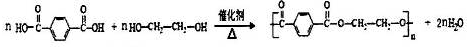 .
.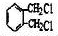 .
.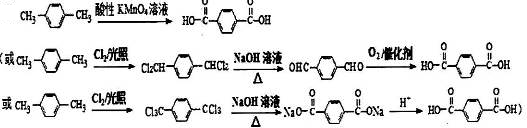 (有机物用结构简式表示,无机试剂任选).
(有机物用结构简式表示,无机试剂任选).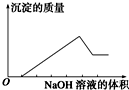 某无色溶液只可能含有以下几种离子:①Mg2+、②Al3+、③Fe2+、④H+、⑤HCO3-、⑥Cl-、⑦OH-.向其中缓慢地滴入NaOH溶液至过量,产生沉淀的质量与加入NaOH溶液的体积的关系如图所示,由此可确定原溶液中一定含有的离子是( )
某无色溶液只可能含有以下几种离子:①Mg2+、②Al3+、③Fe2+、④H+、⑤HCO3-、⑥Cl-、⑦OH-.向其中缓慢地滴入NaOH溶液至过量,产生沉淀的质量与加入NaOH溶液的体积的关系如图所示,由此可确定原溶液中一定含有的离子是( )