题目内容
3.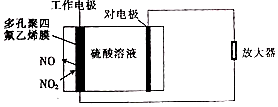 环境监察局常用“定电位”NOx传感器来监测化工厂的氮氧化物气体是否达到排放标准,其工作原理如图所示.下列说法不正确的是( )
环境监察局常用“定电位”NOx传感器来监测化工厂的氮氧化物气体是否达到排放标准,其工作原理如图所示.下列说法不正确的是( )| A. | “对电极”是负极 | |
| B. | “工作电极”上发生的电极反应为NO2+2e-+2H+═NO+H2O | |
| C. | 传感器工作时H+由工作电极移向对电极 | |
| D. | 对电极的材料可能为活泼金属锌 |
分析 “工作电极”通入NO2生成NO,说明NO2被还原,为原电池正极,则“对电极”是负极,原电池工作时,阳离子向正极移动,阴离子向负极移动,以此解答该题
解答 解:A.根据以上分析,“对电极”是负极,故A正确;
B.“工作电极”通入NO2生成NO,为原电池正极,电极方程式为NO2+2e-+2H+═NO+H2O,故B正确;
C.阳离子向正极移动,所以传感器工作时H+由工作电极移向“工作电极”,故C错误;
D.根据以上分析,“对电极”是负极,则对电极的材料可能为活泼金属锌,故D正确.
故选C.
点评 本题考查原电池知识,为高考常见题型和高频考点,注意把握原电池的工作原理,本题解答的关键是离子的定向移动,以此可确定电源的两极和反应类型,注意体会答题思路,难度中等.

练习册系列答案
相关题目
13.NA表示阿伏伽德罗常数,则下列说法正确的是( )
| A. | 1 L 0.1 mol/LNaHSO4溶液中含有0.1 NA个HSO4- | |
| B. | 已知反应:5Cl-+ClO3-+6H+=3Cl2+3H2O,每生成71g Cl2,则转移2NA个电子 | |
| C. | 乙烯(C2H4)和环丙烷(C3H6)组成的28g混合气体中含有氢原子数为4NA个 | |
| D. | 标准状况下,22.4LCCl4中含有NA个CCl4分子 |
11.某有机物的结构简式如下,下列关于该有机物的说法中错误的是( )


| A. | 分子式为C14H18O6 | B. | 含有羟基、羧基和苯基 | ||
| C. | 能发生取代反应 | D. | 能使溴的水溶液褪色 |
18.化学与生活密切相关,下列说法错误的是( )
| A. | 冬季烧煤炭供热取暖与雾霾的形成无必然联系 | |
| B. | 食品包装袋中充人氮气可防腐 | |
| C. | 钢铁表面镀锌可防止铁的腐蚀 | |
| D. | 回收地沟油制造生物柴油符合环境保护的要求 |
4.能用于鉴别Na2CO3固体和NaHCO3固体的方法是( )
| A. | 加稀盐酸 | B. | 加NaOH溶液 | C. | 焰色反应 | D. | 加热 |

