题目内容
海水中含有丰富的镁资源.工业上常用海水晒盐后的苦卤水提取Mg,流程如图1所示:
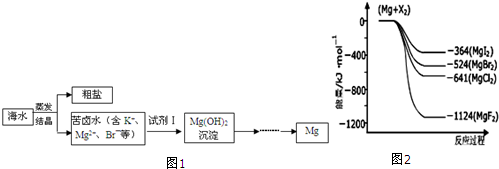
(1)工业制取镁的方法是 法.
(2)试剂Ⅰ一般选用 (填化学式).
(3)图2是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态).
①由图可知Mg与卤素单质的反应均为 (填“放热”或“吸热”)反应;推测化合物的热稳定性顺序为MgI2 MgF2(填“>”、“=”或“<”).
②依图2数据写出MgBr2(s)与Cl2(g)反应的热化学方程式 .
(4)金属Mg与CH3Cl在一定条件下反应可生成CH3MgCl,CH3MgCl是一种重要的有机合成试剂,易与水发生水解反应并有无色无味气体生成.写出CH3MgCl水解的化学方程式 .

(1)工业制取镁的方法是
(2)试剂Ⅰ一般选用
(3)图2是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态).
①由图可知Mg与卤素单质的反应均为
②依图2数据写出MgBr2(s)与Cl2(g)反应的热化学方程式
(4)金属Mg与CH3Cl在一定条件下反应可生成CH3MgCl,CH3MgCl是一种重要的有机合成试剂,易与水发生水解反应并有无色无味气体生成.写出CH3MgCl水解的化学方程式
考点:海水资源及其综合利用
专题:元素及其化合物,化学应用
分析:(1)活泼金属采用电解其熔融盐或氧化物的方法冶炼,如Mg用电解其熔融盐的方法冶炼;
(2)根据从苦卤中提取金属镁的实验操作分析;
(3)①依据图象分析判断,Mg与卤素单质的能量高于卤化物,所以反应是放热反应;物质能量越高越活泼,越不稳定;
②根据盖斯定律构建目标方程式书写;
(4)根据水解其元素的化合价不变分析CH3MgCl水解产物为氢氧化镁、氯化氢和甲烷或Mg(OH)Cl;
(2)根据从苦卤中提取金属镁的实验操作分析;
(3)①依据图象分析判断,Mg与卤素单质的能量高于卤化物,所以反应是放热反应;物质能量越高越活泼,越不稳定;
②根据盖斯定律构建目标方程式书写;
(4)根据水解其元素的化合价不变分析CH3MgCl水解产物为氢氧化镁、氯化氢和甲烷或Mg(OH)Cl;
解答:
解:(1)镁化学性质比较活泼,工业上常用电解熔融氯化镁的方法制取金属镁,反应的化学方程式为:MgCl2(熔融)
Mg+Cl2↑,故答案为:电解;
(2)因为海岸上有丰富的贝壳资源,其主要成分为石灰石,锻烧贝壳可以得到氧化钙,而氧化钙溶于水可制得氢氧化钙溶液,所以试剂Ⅰ应是氢氧化钙溶液其化学式为:Ca(OH)2,故答案为:Ca(OH)2;
(3)①由图象可知,Mg与卤素单质的能量高于卤化物,依据能量守恒判断,反应是放热反应,物质的能量越低越稳定,易图象数据分析,化合物的热稳定性顺序为:MgI2<MgBr2<MgCl2<MgF2,
故答案为:放热;<;
②Mg(s)+Cl2(l)=MgCl2(s)△H=-641kJ/mol,
Mg(s)+Br2(l)=MgBr2(s)△H=-524kJ/mol,
将第一个方程式减去第二方程式得MgBr2(s)+Cl2(g)═MgCl2(s)+Br2(l)△H=-117KJ?mol-1,
故答案为:MgBr2(s)+Cl2(g)═MgCl2(s)+Br2(l)△H=-117KJ?mol-1;
(4)CH3MgCl水解化合价不变,CH3MgCl中,Cl元素的化合价是-1价,H元素的化合价是+1价,C元素的化合价是-4价,镁元素的化合价是+2价,所以CH3MgCl水解生成氢氧化镁、氯化氢和甲烷或Mg(OH)Cl,水解方程式为:CH3MgCl+H2O═CH4↑+Mg(OH)Cl↓或 2CH3MgCl+2H2O═2CH4↑+Mg(OH)2↓+MgCl2,
故答案为:CH3MgCl+H2O═CH4↑+Mg(OH)Cl↓或 2CH3MgCl+2H2O═2CH4↑+Mg(OH)2↓+MgCl2;
| ||
(2)因为海岸上有丰富的贝壳资源,其主要成分为石灰石,锻烧贝壳可以得到氧化钙,而氧化钙溶于水可制得氢氧化钙溶液,所以试剂Ⅰ应是氢氧化钙溶液其化学式为:Ca(OH)2,故答案为:Ca(OH)2;
(3)①由图象可知,Mg与卤素单质的能量高于卤化物,依据能量守恒判断,反应是放热反应,物质的能量越低越稳定,易图象数据分析,化合物的热稳定性顺序为:MgI2<MgBr2<MgCl2<MgF2,
故答案为:放热;<;
②Mg(s)+Cl2(l)=MgCl2(s)△H=-641kJ/mol,
Mg(s)+Br2(l)=MgBr2(s)△H=-524kJ/mol,
将第一个方程式减去第二方程式得MgBr2(s)+Cl2(g)═MgCl2(s)+Br2(l)△H=-117KJ?mol-1,
故答案为:MgBr2(s)+Cl2(g)═MgCl2(s)+Br2(l)△H=-117KJ?mol-1;
(4)CH3MgCl水解化合价不变,CH3MgCl中,Cl元素的化合价是-1价,H元素的化合价是+1价,C元素的化合价是-4价,镁元素的化合价是+2价,所以CH3MgCl水解生成氢氧化镁、氯化氢和甲烷或Mg(OH)Cl,水解方程式为:CH3MgCl+H2O═CH4↑+Mg(OH)Cl↓或 2CH3MgCl+2H2O═2CH4↑+Mg(OH)2↓+MgCl2,
故答案为:CH3MgCl+H2O═CH4↑+Mg(OH)Cl↓或 2CH3MgCl+2H2O═2CH4↑+Mg(OH)2↓+MgCl2;
点评:本题考查了镁的性质、反应热的有关计算、平衡原理等知识点,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握影响沉淀平衡,注意读图的方法,题目难度中等.

练习册系列答案
相关题目
下列关于热化学反应的描述中正确的是( )
| A、已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ?mol-1,则H2SO4和Ba(OH)2反应的反应热△H=2×(-57.3)kJ?mol-1 | ||
B、燃料电池中将甲醇蒸气转化为氢气的热化学方程式是:CH3OH(g)+
则CH3OH(g)的燃烧热为192.9 kJ?mol-1 | ||
| C、H2(g)的燃烧热是285.8 kJ?mol-1,则2H2O(g)═2H2(g)+O2(g)△H=+571.6 kJ?mol-1 | ||
D、葡萄糖的燃烧热是2800 kJ?mol-1,则
|
在密闭容器中发生如下反应:mA(g)+nB(g)?pC(g)达到平衡后,保持温度不变,将气体体积缩小到原来的
,当达到新平衡时,C的浓度为原来的1.9倍.下列说法中正确的是( )
| 1 |
| 2 |
| A、m+n>p |
| B、平衡向逆反应方向移动 |
| C、A的转化率增大 |
| D、C的体积分数增加 |
下列四种溶液:①pH=2的CH3COOH溶液;②pH=2的HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液.
相同条件下,有关上述溶液的比较中,正确的是( )
相同条件下,有关上述溶液的比较中,正确的是( )
| A、由水电离的c(H+):①=②>③=④ |
| B、将①、③两种溶液等体积混合后,pH可能不等于7 |
| C、等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量:②最大 |
| D、向等体积的四种溶液中分别加入100 mL水后,溶液的pH:③>④>①>② |
对于可逆反应:2SO2+O2?2SO3(g)△H<0,升高温度产生的影响为( )
| A、v正增大,v逆减小 |
| B、v正减小,v逆增大 |
| C、v正和v逆不同程度的增大 |
| D、v正和v逆同等程度的增大 |