题目内容
2.汽车尾气是造成雾霾天气的重要原因之一,尾气中的主要污染物为CxHy、NO、CO、SO2及固体颗粒物等.研究汽车尾气的成分及其发生的反应,可以为更好的治理汽车尾气提供技术支持.请回答下列问题:(1)治理尾气中NO和CO的一种方法是:在汽车排气管上装一个催化转化装置,使二者发生反应转化成无毒无污染气体,该反应的化学方程式是2NO+2CO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2.
(2)活性炭也可用于处理汽车尾气中的NO.在1L恒容密闭容器中加入0.1000mol NO和2.030mol固体活性炭,生成A、B两种气体,在不同温度下测得平衡体系中各物质的物质的量以及容器内压强如下表:
| 活性炭/mol | NO/mol | A/mol | B/mol | p/MPa | |
| 200℃ | 2.00 | 0.0400 | 0.0300 | 0.0300 | 3.93 |
| 335℃ | 2.005 | 0.050 | 0.0250 | 0.0250 | p |
(3)汽车尾气中的SO2可用石灰水来吸收,生成亚硫酸钙浊液.常温下,测得某纯CaSO3与水形成的浊液pH为9,已知Kal(H2SO3)=1.8×10-2,Ka2(H2SO3)=6.0×10-9,忽略SO32-的第二步水解,则Ksp(CaSO3)=4.2×10-9.
(4)尾气中的碳氢化合物含有甲烷,其在排气管的催化转化器中可发生如下反应CH4(g)+H20(1)?CO(g)+3H2 (g)△H=+250.1kJ•mol-l.已知CO(g)、H2(g)的燃烧热依次为283.0kJ•mol-1、285.8kJmol-1,请写出表示甲烷燃烧热的热化学方程式CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3KJ/mol.以CH4(g)为燃料可以设计甲烷燃料电池,该电池以稀H2S04作电解质溶液,其负极电极反应式为CH4-8e-+2H2O=CO2+8H+,已知该电池的能量转换效率为86.4%,则该电池的比能量为13.4kW•h•kg-1(结果保留1位小数,比能量=$\frac{电池输出电能(kW•h)}{燃料质量(kg)}$,lkW•h=3.6×1 06J).
分析 (1)已知反应物和生成物,可结合质量守恒定律书写方程式并配平;
(2)碳和一氧化氮反应生成氮气和二氧化碳,反应前后气体的物质的量不变;根据Kp=$\frac{c({N}_{2})c(C{O}_{2})}{{c}^{2}(NO)}$;
(3)常温下,测得某纯CaSO3与水形成的浊液pH为9,由可知CaSO3(s)?Ca2+(aq)+SO32-(aq),且SO32-+H2O?HSO3-+OH-,由Ka2(H2SO3)=6.0×10-9可知SO32-+H2O?HSO3-+OH-的水解Kh=$\frac{1{0}^{-14}}{6×1{0}^{-9}}$=1.67×10-4,以此计算c(SO32-),溶液中c(Ca2+)=c(SO32-)+c(HSO3-),结合Ksp(CaSO3)=c(Ca2+)×c(SO32-)计算;
(4)根据盖斯定律解题;CH4燃料电池中,CH4从负极通入,在反应中失电子被氧化,酸性条件下生成二氧化碳和水;设燃料为1kg计算.
$\frac{电池输出电能(kW•h)}{燃料质量(kg)}$.
解答 解:(1)在催化剂条件下NO和CO反应,生成CO2和N2,反应的方程式为2NO+2CO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2,
故答案为:2NO+2CO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2;
(2)碳和一氧化氮反应生成氮气和二氧化碳:C+2NO?N2+CO2;反应前后气体的物质的量不变,温度升高压强增大;Kp=$\frac{c({N}_{2})c(C{O}_{2})}{{c}^{2}(NO)}$=$\frac{0.03×0.03}{0.0{4}^{2}}$=0.5625,
故答案为:C+2NO?N2+CO2;>;0.5625;
(3)由Ka2(H2SO3)=6.0×10-9可知SO32-+H2O?HSO3-+OH-的水解Kh=$\frac{1{0}^{-14}}{6×1{0}^{-9}}$=1.67×10-4,
常温下,测得某纯CaSO3与水形成的浊液pH为9,c(HSO3-)=c(OH-)=1×10-5,
可知c(SO32-)=$\frac{(1×1{0}^{-5})^{2}}{1.67×1{0}^{-4}}$=6×10-5,
又c(Ca2+)=c(SO32-)+c(HSO3-)=7×10-5,
Ksp(CaSO3)=c(Ca2+)×c(SO32-)=7×10-5×6×10-5=4.2×10-9,
故答案为:4.2×10-9;
(4)①CH4(g)+H2O(1)?CO(g)+3H2 (g)△H=+250.1kJ.mol-l
②CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-283.0kJ/mol
③H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8kJ•mol-1
①+②+③×3得CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3KJ/mol,
在CH4燃料电池中,负极上是燃料CH4发生失电子的氧化反应,在酸性环境下,电极反应为CH4-8e-+2H2O=CO2+8H+;
设燃料为1kg,放出的能量为$\frac{1000}{16}$×890.3KJ×86.4%=4.81×107J;比能量为$\frac{4.81×1{0}^{7}J}{3.6×1{0}^{6}J}$=13.4,
故答案为:CH4(g)+2O2(g)→CO2(g)+2H2O(l)△H=-890.3KJ/mol;CH4-8e-+2H2O=CO2+8H+;13.4.
点评 本题综合考查难容电解质的溶解平衡以及弱电解质的电离、CH4燃烧热的热化学方程式书写、原电池原理的应用,主要考查了燃料电池的电极方程式的书写,题目难度不大,注意电解质溶液的酸碱性对电极方程式的影响.

| A. | Ba( NO3-)2=Ba2++( NO3-) 2 | B. | NaHSO4=Na++H++SO42- | ||
| C. | H2SO4=2H++SO42- | D. | KClO3=K++ClO3- |
| A. | 这个反应是氧化还原反应 | B. | 制造过程中元素种类发生改变 | ||
| C. | 另一种化合物为NaCl | D. | 金刚石属于金属单质 |
| A. | 氧化铝 | B. | 氢氧化铝 | C. | 铝 | D. | 碳酸氢钠 |

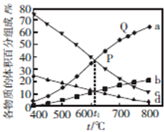 CO2与H2合成甲醚的主要反应如下:
CO2与H2合成甲醚的主要反应如下: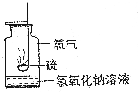 郑州一中是一所具有丰厚的历史积淀、独特的精神内涵,以关注学生智慧与灵魂为学校文化内核,充满创新精神,能够培养具有国际视野的拔尖人才,拥有核心竞争力的国内名校.目前一中教育集团包含小学部、初中部、高中部三个学部的十余所学校.学校以主体课堂教学为载体,以培养学生的创新思维和实践能力为目标,在教学活动中特别注重学生科学素养的提升,如对于I A和ⅥA族重要元素化合物的性质,各校区根据实际情况开展了丰富多彩的探究活动.
郑州一中是一所具有丰厚的历史积淀、独特的精神内涵,以关注学生智慧与灵魂为学校文化内核,充满创新精神,能够培养具有国际视野的拔尖人才,拥有核心竞争力的国内名校.目前一中教育集团包含小学部、初中部、高中部三个学部的十余所学校.学校以主体课堂教学为载体,以培养学生的创新思维和实践能力为目标,在教学活动中特别注重学生科学素养的提升,如对于I A和ⅥA族重要元素化合物的性质,各校区根据实际情况开展了丰富多彩的探究活动. .
.