题目内容
20.短周期主族元素X、Y、Z原子序数之和为28,X+与Z2-具有相同的核外电子层结构,Y、Z在同一周期.下列推测不正确的是( )| A. | 元素Y的最高价氧化物的水化物是强酸 | |
| B. | 三种元素的原子半径:r(X)>r(Z)>r(Y) | |
| C. | Y的简单气态氢化物的热稳定性比Z的强 | |
| D. | 由X与Z两种元素组成的离子化合物不止一种. |
分析 X+与Z2-具有相同的核外电子层结构,Y、Z在同一周期.可推X在Y、Z的下一个周期,则X为Na、Z为O、进而可知Y为F,结合元素周期律的递变规律解答该题.
解答 解:X+与Z2-具有相同的核外电子层结构,Y、Z在同一周期.可推X在Y、Z的下一个周期,则X为Na、Z为O、进而可知Y为F,
A.Y为F,没有正价,不存在最高价氧化物的水化物,故A错误;
B.原子半径Na的最高,同周期元素从左到右原子半径逐渐减小,O>F,故B正确;
C.非金属性F>O,元素的非金属性越强,对应的氢化物越稳定,故C正确;
D.可形成Na2O、Na2O2等化合物,故D正确.
故选A.
点评 本题考查元素的推断和元素周期律,为高考常见题型,题目难度中等,注意把握元素的推断的角度以及元素周期律的递变规律.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
10.25℃,加水将10mL pH=11的氨水稀释至1L,则下列判断中正确的是( )
| A. | 稀释后溶液的pH=9 | |
| B. | 稀释过程中,溶液中所有离子的浓度均减小 | |
| C. | 稀释后溶液中$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}.{H}_{2}O)}$减小 | |
| D. | 该氨水稀释前后中和盐酸的能力相同 |
11.下列有关实验的操作和结论正确的是( )
| A. | 明矾和漂白粉均可用于自来水的杀菌、消毒 | |
| B. | 用丁达尔实验可以将Al(OH)3胶体和NaCl溶液区分 | |
| C. | CCl4萃取碘水中的I2,先从分液漏斗下口放出有机层,后从分液漏斗下口放出水层 | |
| D. | 浓盐酸与MnO2反应制备纯净Cl2,气体产物先通过浓硫酸,后通过饱和食盐水 |
8.如图为氢氧燃料电池的构造示意图.下列说法不正确的是( )
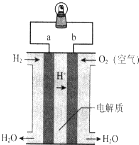

| A. | a电极是正极 | B. | 电流由b通过灯泡流向a | ||
| C. | 该电池总反应是2H2+O2═2H2O | D. | 该装置可将化学能转化为电能 |
15.下列关于酯化反应说法正确的是( )
| A. | 用CH3CH218OH与CH3COOH发生酯化反应,生成H218O | |
| B. | 反应液混合时,顺序为先倒乙醇再倒浓硫酸最后倒乙酸 | |
| C. | 乙酸乙酯不会和水生成乙酸和乙醇 | |
| D. | 用蒸馏的方法从饱和Na2CO3溶液中分离出乙酸乙酯 |
5.等温、等压下,Ag CO2所占的体积为11.2L,0.5A g X的气体所占的体积为7.7L,则气体的相对分子质量为( )
| A. | 16 | B. | 32 | C. | 48 | D. | 64 |
12.当氨完全分解成氮气和氢气时,混合气体对空气的相对密度为( )
| A. | 1.17 | B. | 0.74 | C. | 0.293 | D. | 1.03 |
 .
.